Воспаление легких, которое также называют пневмонией, — патологический процесс, поражающий ткани легких. Встречается такая патология как у взрослых, так у детей. Воспаление легких нуждается в неотложном лечении, даже если протекает не в тяжелой форме. Причиной пневмонии преимущественно выступает инфекция — поражение легкого патогенными микроорганизмами. Поэтому применение антибиотиков при пневмонии у взрослых и детей в комплексе с дополнительными препаратами — основа лечения.
Содержание
Общие принципы применения антибиотиков при воспалении легких
Антибиотики при воспалении легких: виды и формы
Полусинтетические пенициллины
Макролиды
Цефалоспорины
Фторхинолоны
Карбапенемы
Монобактамы
Общие принципы применения антибиотиков при воспалении легких
Пациент без медицинского образования не знает наверняка, какие антибактериальные препараты ему помогут при воспалении легких.
| Для того чтобы лечение антибиотиками было максимально быстрым и эффективным, нужно обратиться к доктору. Врачи придерживаются определенных правил лечения пневмонии. Перед тем как выписать антибиотики, специалист направляет пациента на исследования и анализы. |
В первую очередь как взрослым, так и детям нужно сделать рентгенографию грудной клетки. После подтверждения диагноза «воспаление легких» пациенту необходимо сдать биоматериал (мокроту) на анализ. Бактериологический посев и антибиотикограмма выполняется 5-7 дней, так что результаты нужно будет подождать. Бакпосев дает возможность выявить, какой именно микроорганизм в легких стал причиной развития пневмонии. Проведение антибиотикограммы позволяет определить чувствительность патогена к различным препаратам. Так специалист выяснит, какие антибиотики будут для данного пациента наиболее эффективны. Кроме того, лабораторное исследование мокроты позволяет исключить грибковую природу воспаления легких, туберкулез. В случае подозрений на смешанную природу пневмонии специалист может назначить комбинацию антибиотиков и противовирусных средств.
На практике в большинстве случаев недопустимо ждать результатов анализов, так как воспаление легкого может быстро привести к дыхательной недостаточности, поэтому при пневмонии назначается антибиотик с широким спектром действия. После получения результатов анализа экссудата легких при необходимости препарат можно заменить.
Существует перечень клинических и лабораторных признаков, которые позволяют врачу оценить результативность лечения пневмонии:
● температура тела снижается;
● более слабые симптомы интоксикации;
● дыхательная недостаточность и одышка менее интенсивны, так как повышается сатурация кислорода;
● снижение количества выделяемой мокроты и изменение ее цвета.
Эффективность лечения пневмонии оценивается через 48-72 часа после начала применения антибиотиков. Одновременно у пациента сохраняются субфебрильная температура, хрипы в груди, кашель, слабость, повышенное потоотделение и остаточные следы пневмонии на рентгенограмме. Несмотря на улучшение общего состояния пациента, отменять применяемые антибиотики или менять их на другой подвид нельзя. Рекомендованный курс антибиотиков очень важно пройти в полном объеме, согласно назначению доктора. Это не позволит патогенным микроорганизмам выработать к антибиотикам резистентность и не допустит развития осложнений патологии легких в ближайшем будущем.
Антибиотики при воспалении легких: виды и формы
Раньше пораженные инфекцией легкие лечили преимущественно природным антибиотиком пенициллиновой группы, так как не было другой альтернативы. Однако у естественных пенициллинов есть побочные эффекты, что крайне нежелательно при воспалительном процессе в легких. Также они воздействуют на достаточно узкий спектр патогенов, к тому же, быстро развивается устойчивость к антибиотикам. Поэтому ученые разработали более современные средства, которые в настоящее время широко применяются для эффективной и безопасной терапии воспаления легких как у детей, так и у взрослых.
Условно антибиотики при пневмонии подразделяются на несколько групп: ● полусинтетические пенициллины;
● макролиды;
● цефалоспорины;
● фторхинолоны;
● карбапенемы;
● монобактамы.
Для удобства применения у взрослых и детей противомикробные средства выпускаются в разных лекарственных формах. Для взрослых — это таблетки и капсулы, детям с поражением нижних дыхательных путей назначаются суспензии. Инъекционные формы применяются в любом возрасте, однако в силу инвазивности процедуры при терапии взрослых они применяются чаще.
Полусинтетические пенициллины
Усовершенствованные пенициллины более результативны при пневмониях, чем их предшественники. В спектр противомикробной активности полусинтетических пенициллинов входит большинство грамположительных бактерий, гемофильная палочка и пневмококки. При терапии неосложненной пневмонии антибиотиком используется преимущественно эта группа. Несомненный плюс полусинтетических пенициллинов — их низкая токсичность по сравнению с другими группами антибактериальных средств. Именно поэтому данная группа препаратов часто используется в лечении воспалений не только у взрослых, но и у детей, беременных женщин.
К пенициллиновым антибиотикам относятся оксациллин и клоксациллин, которые наиболее результативно и быстро действуют при пневмониях, вызванных стафилококками.
Расширенными антимикробными свойствами обладают аминопенициллины — амоксициллин и ампициллин. Они широко применяются у взрослых при внебольничных пневмониях. Препараты амоксициллина представлены торговыми названиями «Флемоксин Солютаб», «Хиконцил», «Оспамокс».
В отдельную группу следует выделить комбинированные ингибиторозащищенные антибиотики. Помимо основного действующего вещества (антибиотика), они содержат вспомогательные компоненты, которые усиливают лечебный эффект, обеспечивая антибиотику защиту от бета-лактамаз — агрессивных ферментов, выделяемых вредоносными бактериями. Самые популярные антибиотики при пневмонии из группы комбинированных защищенных пенициллинов — «Аугментин» и «Флемоклав Солютаб». Они содержат в себе комбинацию амоксициллина и клавулановой кислоты, сочетание которых позволяет эффективно устранить бактериальное инфицирование легкого.
Терапия пневмонии пенициллиновыми препаратами может вызвать ряд побочных эффектов — аллергическую реакцию, расстройство желудка, колит и различные диспепсические явления.
Макролиды
Наиболее часто группа макролидов назначается как препараты первой линии, если у пациента есть индивидуальная непереносимость пенициллинов. Этим антибиотикам свойственна активность при атипичных формах болезни, причиной которых выступают внутриклеточные мембранные паразиты (клебсиеллы, легионеллы), хламидии, микоплазмы и гемофильная палочка. Также макролиды эффективны против грамположительных кокков.
Для лечения воспалительного процесса в легких используются кларитромицин («Клацид», «Кларитромицин-Тева», «Фромилид») и азитромицин («Азитрал», «Сумамед», «Азитрокс»).
«Азитрал» выпускается в таблетках с дозировкой для взрослых 250 или 500 мг. Применяется однократно в сутки за два часа до или после приема пищи.
«Сумамед» и «Азитрокс» выпускаются в таблетках и капсулах для взрослых по 500 мг (принимать один раз в сутки), а также в порошке для детской суспензии.
«Клацид» имеет три формы выпуска — гранулы для приготовления суспензий, порошок для изготовления инфузии и таблетки. Пероральное применение препарата при пневмонии осуществляется дважды в сутки курсом до двух недель.
«Фромилид» в таблетках по 500 мг два раза в сутки назначается взрослым пациентам при инфекционном поражении легких. Препарат необходимо принимать две недели, не прерывая курс и не меняя тип антибиотика.
Иногда для лечения инфекций нижних дыхательных путей применяется первый противомикробный препарат из группы макролидов — «Эритромицин». Он широко используется для терапии атипичных форм болезни, вызванных легионеллами, которые отличаются высокой степенью летальности. «Эритромицин» нужно принимать каждые 6 часов по 400-500 мг. При пневмонии неосложненного течения длительность терапии «Эритромицином» обычно составляет от семи до десяти дней. Недостатком данного препарата можно назвать частые побочные эффекты после его применения, как правило, со стороны желудочно-кишечного тракта. Они обусловлены способностью макролидов усиливать моторику кишечника.
Цефалоспорины
Группа цефалоспоринов обычно применяется, если у пациента доказана индивидуальная непереносимость макролидов. Как правило, цефалоспорины обеспечивают лечение пневмонии на неосложненной стадии. Они используются при терапии инфекционных процессов, вызванных пневмококками, стрептококками и энтеробактериями.
К антибиотикам первого поколения цефалоспоринов, которые применяются в борьбе с инфекциями нижних дыхательных путей, относят «Цефапирин», «Цефалексин» и «Цефазолин».
Второе поколение включает в себя «Цефуроксим» и «Цефокситин», которые используются для лечения инфекций, вызванных клебсиеллой, кишечной и гемофильной палочками. «Цефокситин» при пневмониях чаще назначается ступенчато: сначала инъекционно, а при улучшении состояния — перорально.
Третье поколение представлено «Цефотаксимом» и «Цефтазидимом», «Цефтриаксоном», «Цефоперазоном», которые обладают широкой антибактериальной активностью. Они справляются со всеми патогенными бактериями, кроме энтерококков и некоторых стафилококков. Существует комбинированный препарат «Цефоперазон» с сульбактамом, активный в отношении бактерий, содержащих фермент бета-лактамазу, разрушающую антибактериальное вещество. Такие препараты используются для лечения воспалительных процессов легких в тяжелых случаях.
Четвертое поколение включает в себя цефепим (торговые названия — «Максипим», «Максицеф», «Цепим», «Ладеф») и цефпиром («Кейтен», «Цефанорм»). Они наиболее эффективны против грамположительных и грамотрицательных аэробных и анаэробных микроорганизмов, при осложнениях пневмоний в виде плевритов и абсцессов.
Цефалоспорины применяются для лечения тяжелой и крайне тяжелой степеней пневмонии. Как правило, в этих целях используются препараты третьего и четвертого поколения, которые обладают выраженным бактерицидным эффектом (происходит абсолютное уничтожение клеток болезнетворных бактерий). Терапия пациентов с тяжелой пневмонией проводится в стационаре.
Среди представителей третьего поколения цефалоспоринов используются и парентеральные, и пероральные формы лекарственных средств. В форме капсул по 400 мг выпускаются препараты цефиксима («Супракс») и цефтибутена («Цедекс»). Их нужно принимать один раз в сутки. В форме таблеток по 200 или 400 мг выпускается препарат цефдиторена («Спектроцеф»), который нужно принимать дважды в сутки.
Из третьего поколения можно выделить инъекционные формы цефтриаксона («Азаран»). Он выпускается в форме порошка для приготовления инъекционного раствора по 1 грамму. Назначается внутримышечно в растворе с 1% лидокаином один или два раза в сутки (в зависимости от назначения доктора). Парентеральные препараты, обладающие дополнительными свойствами против синегнойной палочки при пневмониях, — цефтазидим («Фортум» — назначается в/в или в/м до шести грамм в день в два-три применения) и цефоперазон («Цефобид» — назначается до четырех грамм в день, разделенных на два приема).
| Лекарственные средства группы цефалоспоринов обычно хорошо переносятся человеческим организмом. Исключения могут составить пациенты с тяжелой почечной или печеночной недостаточностью, а также пожилые люди. |
Фторхинолоны
Применение фторхинолоновой группы обычно рекомендуют при аллергической реакции на все остальные средства. Фторхинолоны используются для лечения тяжелых форм инфекций нижних дыхательных путей. Эти вещества быстро всасываются в клетки и способны бороться с пневмококками, стафилококками, грамотрицательными бактериями и атипичными возбудителями пневмоний. Благодаря широкому спектру противомикробной активности данная лекарственная группа отлично справляется с терапией практически всех форм внегоспитальных пневмоний. Однако использование ранних фторхинолонов при внебольничных воспалениях нижних дыхательных путей было ограничено, так как они были практически не результативны против основного возбудителя — пневмококка.
В качестве действующего вещества для терапии патологий нижних дыхательных путей, которые вызваны не пневмококком, чаще всего выступают офлоксацин («Зофлокс», «Таривид») и ципрофлоксацин («Ципробай», «Цифран»).
Из нового поколения фторхинолонов можно выделить левофлоксацин («Глево», «Лебел», «Левоксимед», «Леволет», «Левофлокс»), который высокоактивен против пенициллинрезистентного пневмококка. Левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения, поэтому применяется как для амбулаторного лечения, так и для пациентов в стационаре. Клинические исследования подтверждают высокую эффективность и хорошую переносимость левофлоксацина, вводимого при внебольничных пневмониях по 0,5 г однократно в сутки.
Второй современный препарат из группы фторхинолонов — спарфлоксацин («Спарфло», «Флоксимар»). В России данное вещество выпускается только в пероральной форме. Несмотря на высокую антибактериальную эффективность, спарфлоксацин обладает сильно выраженным побочным действием — фототоксичностью (повышенная чувствительность кожи к влиянию ультрафиолетовых лучей). Помимо этого, он нередко вызывает и другие нежелательные эффекты, что делает его не рекомендованным для рутинного применения в амбулаторной практике. Потому спарфлоксацин применяется для терапии пневмоний только при отсутствии альтернатив.
Одни из новейших антибиотиков группы фторхинолонов — моксифлоксацин («Авелокс», «Моксифлокс») и гатифлоксацин («Озерлик», «Гатилин», «Гатимак»). Они обладают высокой активностью в отношении грамположительных, атипичных и анаэробных микроорганизмов. Относятся к группе «респираторных фторхинолонов». В клинических исследованиях показывают высокую результативность и хорошую переносимость.
Карбапенемы
Карбапенемы — еще одна из «запасных» групп в лечении воспалений нижних дыхательных путей в условиях стационара. Препараты обладают широким спектром активности, меньшей устойчивостью к бета-лактамазам, чем цефалоспорины и пенициллины. Назначаются при осложненных формах пневмоний и септических процессах. Бактериальная активность карбапенемов больше зависит от кратности применения, чем от пиковой концентрации в организме. Они представлены такими действующими веществами, как имипенем, меропенем и дорипенем.
Среди антибиотиков представлены такие торговые названия:
● имипенем+циластатин («Тиенам», «Аквапенем», «Циласпен», «Гримипенем») применяется внутримышечно и внутривенно капельно;
● меропенем («Дженем») выпускается в форме порошка для в/в введения раствора до 1 г каждые 8 часов.
Несмотря на все преимущества антибиотиков группы карбапенемов во время лечения нозокомиальных инфекций, они обладают и недостатками, например, отсутствием активности против атипичной микрофлоры.
Монобактамы
Группу монобактамов также называют моноциклическими бета-лактамами. Из этой группы антибиотиков в клинической практике в настоящее время применяется только одно вещество — азтреонам. Оно обладает весьма узким спектром противомикробной активности и применяется для лечения инфекций, которые вызваны аэробной и грамотрицательной флорой. Бактерицидный эффект азтреонама обусловлен нарушением синтеза клеточной стенки патогена. Его своеобразие объясняется устойчивостью препарата к разрушительному воздействию бета-лактамазами, вырабатываемыми аэробной грамотрицательной флорой, однако к аналогичным ферментам стафилококков и бактероидов этот препарат неустойчив.
Клиническое значение имеет результативность азтреонама в отношении микроорганизмов семейства энтеробактерий (кишечной палочки, клебсиеллы, протея, морганеллы, цитробактер), синегнойной палочки и нозокомиальных (внутрибольничных) штаммов, которые устойчивы к аминогликозидам, цефалоспоринам и уреидопенициллинам. Азтреонам не обладает губительным влиянием на ацинетобактер, грамположительные кокки и анаэробные микроорганизмы.
Препарат применяется исключительно парентерально, хорошо распределяется в тканях и средах человеческого организма. Из нежелательных побочных реакций можно выделить расстройства со стороны ЖКТ (дискомфорт в животе, диарея, рвота) и ЦНС (головокружение, головная боль, бессонница).
Также возможны аллергические реакции (сыпь, крапивница) на лекарство, которые возникают значительно реже, чем от других бета-лактамных препаратов. Ввиду возможного антагонизма, азтреонам не рекомендуется комбинировать с карбапенемами.
Здесь недопустимо самолечение, но если у вас есть рецепт от врача, нужный препарат можно купить в сети аптек «Ригла».
АНТИБИОТИКИ в лечении острых бронхитов у детей
Какова основная этиологическая причина острых и рецидивирующих бронхитов?
Какова тактика выбора антибактериальных препаратов?
Бронхит является одним из самых распространенных инфекционных заболеваний респираторного тракта у детей и, казалось бы, не представляет особой проблемы для врача-педиатра. Однако это весьма обманчивое впечатление. Существует множество нерешенных вопросов, связанных с терминологией, этиологией и патогенезом этого заболевания, а также влиянием экологических, аллергических и иных агрессивных факторов. Все это создает ряд объективных трудностей и в интерпретации клинических данных, и в выборе тактики терапии.
Прежде всего остановимся на определении понятий. В настоящее время принято выделять три клинические формы бронхита: острый, рецидивирующий и хронический [5]. Острый бронхит встречается в любом возрастном периоде жизни человека и представляет собой острое самокупирующееся (т. е. самоизлечивающееся) воспаление слизистой оболочки трахеобронхиального дерева, обычно завершающееся полным излечением и восстановлением функций [6]. Чаще всего острый бронхит является одним из проявлений острого респираторного заболевания различной этиологии — вирусной, бактериальной, грибковой, паразитарной, смешанной. Существует также острый ирритативный бронхит химической, аллергической и другой неинфекционной природы.
Острый бронхит, если он не сопровождается клинически выраженными признаками обструкции, принято обозначать как острый простой бронхит, или просто острый бронхит.
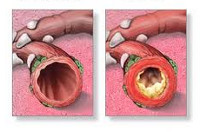
В отличие от него острый обструктивный бронхит характеризуется тем, что воспаление слизистой оболочки бронхов сопровождается сужением и/или закупоркой дыхательных путей за счет отека и гиперплазии слизистой оболочки, гиперсекреции слизи или развития бронхоспазма. Возможен сочетанный характер бронхообструкции. Обструктивный бронхит несколько чаще регистрируется у детей раннего возраста, т. е. у детей до 3 лет. Причем в этом возрасте обструктивный синдром преимущественно обусловлен гиперсекрецией вязкой и густой слизи и гиперплазией слизистой оболочки. Бронхоспазм более характерен для детей старше 4 лет [1].
Одной из клинических форм острого воспаления слизистой оболочки бронхов является бронхиолит. Он, по сути, представляет собой клинический вариант острого обструктивного бронхита, но в отличие от последнего характеризуется воспалением слизистых оболочек мелких бронхов и бронхиол. Этим определяются клинические особенности заболевания, его тяжесть и прогноз. Бронхиолит встречается преимущественно у детей раннего возраста, причем чаще в грудном возрасте, т. е. до года [1, 5].
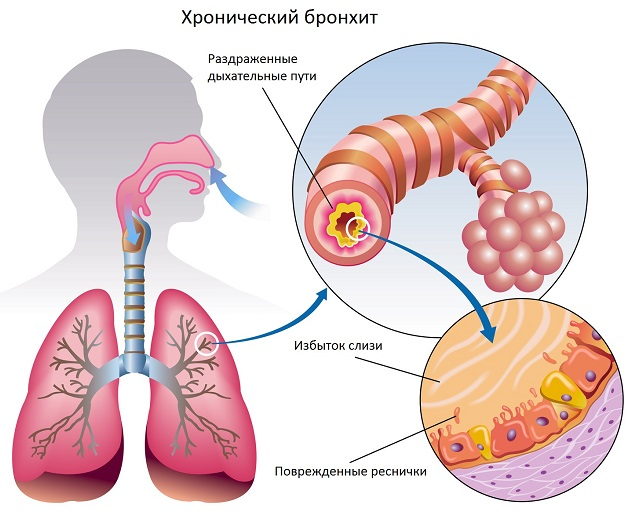
Под рецидивирующим бронхитом понимают такую форму заболевания, когда в течение года отмечается не менее трех эпизодов острого бронхита. Как правило, подобная склонность к развитию повторного воспаления слизистой бронхов не случайна, и в основе ее лежит снижение мукоцилиарного клиренса вследствие поражения мерцательного эпителия: повышенной вязкости слизи; изменения диаметра бронхов; увеличения резистентности респираторных путей; нарушения местной или общей противоинфекционной защиты.
Рецидивирующий бронхит клинически протекает в виде острого простого или обструктивного бронхитов, реже в виде эпизодов повторного бронхиолита. У детей рецидивирующий бронхит встречается в любом возрастном периоде детства, но наиболее часто регистрируется после 3 лет.
Терапия любого инфекционного заболевания и, в частности, выбор антибактериальной терапии, как известно, определяются этиологией процесса.
Причинами острого и рецидивирующего бронхитов в подавляющем большинстве случаев являются инфекционные агенты: вирусы, вирусно-бактериальные ассоциации и бактерии. Значительно менее распространены неинфекционные факторы: химические, физические, аллергические. Последние могут выступать как самостоятельные причинные факторы либо обуславливать предрасположение к развитию инфекционного воспалительного процесса или отягощать его течение.
Среди вирусов ведущее место занимают 1 и 3-й типы парагриппа, РС-вирус, аденовирусы. Реже в качестве причины бронхитов выступают риновирусы, вирусы гриппа, энтеровирусы, вирус кори, цитомегаловирус и др. Однако забывать об их этиологической значимости не следует.
Возрастной и эпидемиологический аспекты играют в развитии бронхита немаловажную роль. Такие вирусы, как парагрипп, аденовирус, риновирус, вирус гриппа практически с одинаковой частотой вызывают бронхит в любом возрасте. Здесь наибольшую значимость имеет эпидемиологическая ситуация: время года (преимущественно холодный период), «скученность» (проживание в общежитии, частое использование общественного транспорта, пребывание в детском коллективе и т. д.), эпидемия и т. д.
Риносинтициальный вирус как причина бронхита чаще встречается у детей раннего возраста, в основном от 6 месяцев до 3 лет, что, видимо, связано с определенным тропизмом этого возбудителя. При этом сезонность и «скученность» играют в развитии заболевания значительно меньшую роль.
Вид вирусной инфекции оказывает существенное влияние на характер поражения слизистой. Так, для парагриппа, гриппа, цитомегаловирусной инфекции характерны дистрофия и деструкция эпителия с отторжением целых слоев. Для РС-вирусной инфекции — гиперплазия эпителия мельчайших бронхов и бронхиол, подушкообразное разрастание эпителия с нарушением бронхиальной проводимости. Именно с этим связывают тот факт, что при РС-вирусной инфекции чаще развивается бронхиолит или острый обструктивный бронхит. Аденовирусная инфекция сопровождается выраженным экссудативным компонентом, нередко наблюдаются слизистые наложения, разрыхление и отторжение эпителия, имеет место образование в стенке бронха крупноклеточных инфильтратов. Это способствует формированию ателектазов и обструкции дыхательных путей.
Как отмечалось выше, вирусы могут быть самостоятельной причиной болезни. По нашим данным, у детей старше 4 лет вирусные бронхиты регистрируются примерно в 20% случаев, но у детей от 14 дней до 4 лет менее чем в 10% случаев. Роль вирусов в целом в этиологии инфекций трахеобронхиального дерева в этой возрастной группе оказалась невысока — до 15%. Как правило, они встречались в ассоциациях, чаще — с бактериями, реже — с другими представителями микробного мира: грибами, простейшими [7, 8].
Бактерии, способные становиться причиной острого бронхита, также весьма разнообразны. Причем этиологическая структура острых внебольничных и внутрибольничных заболеваний существенно различается. В этиологии внебольничных бронхитов, т. е. бронхитов, развившихся в обычных условиях жизни ребенка, принимает участие довольно большой спектр возбудителей.
В настоящее время в зависимости от характера клинических проявлений внебольничные бронхиты, так же как и пневмонии, принято делить на типичные и атипичные.
Для типичных бронхитов характерно острое начало с выраженной лихорадочной реакцией, интоксикацией, кашлем и довольно выраженными физикальными проявлениями. Типичные бронхиты обычно обусловлены пневмококком, моракселлой катарралис и гемофильной палочкой.
Для атипичных заболеваний трахеобронхиального дерева характерно малосимптомное подострое начало, с нормальной или субфебрильной температурой, отсутствием интоксикации. Самым типичным симптомом является сухой непродуктивный навязчивый кашель. Причинами атипичных внебольничных бронхитов являются хламидия пневмонии и микоплазма пневмонии [6, 7, 8]. При микоплазменной этиологии заболевания в его дебюте может отмечаться респираторный синдром при нормальной или субфебрильной температуре. При хламидийной, особенно у детей первых месяцев жизни, в половине случаев встречается конъюнктивит, а кашель носит коклюшеподобный характер.
Наблюдения зарубежных авторов и наши исследования, проведенные в 1996-1999 гг., свидетельствуют, что этиологическая значимость хламидий и микоплазм, являющихся внутриклеточными возбудителями инфекций, значительно выше, чем предполагалось ранее. Микоплазменная и хламидийная этиология бронхита и пневмонии у детей в настоящее время может составлять от 25 до 40%, причем она наиболее высока в первый год жизни и после 10 лет [7, 8].
Особенностью внутриклеточных возбудителей является их нечувствительность к традиционной антибактериальной терапии, что наряду с недостаточностью макрофагального звена защиты, характерной для этой инфекции, способствует затяжному и рецидивирующему течению воспалительного процесса в бронхах. Определенную роль играет и тот факт, что в окружении ребенка, как правило, имеются носители данного инфекционного агента, и это создает условия для реинфицирования. Поэтому микоплазменные и хламидийные бронхиты нередко приобретают затяжное (до 4-8 недель) или рецидивирующее течение.
Лечение острого бронхита в лихорадочный период болезни включает постельный режим, обильное питье, назначение жаропонижающих и противовоспалительных средств. Отдельным направлением является выбор противокашлевой терапии.
Но наиболее сложным следует признать вопрос о назначении и выборе антибактериальной терапии.
Большая значимость вирусов в этиологии болезни, преобладание легких форм, самокупирующийся характер заболевания ставят вопрос о целесообразности использования антибиотиков в терапии острых бронхитов. И вопрос этот широко обсуждается. Ряд исследований, проведенных на взрослых больных, свидетельствуют о том, что использование антибактериальной терапии не оказывает существенного влияния на исходы бронхита [4]. Это ставит под сомнение необходимость ее применения.
С другой стороны, по данным, приведенным в Государственном докладе о состоянии здоровья населения России [2], заболевания органов дыхания остаются ведущей причиной смерти детей первого года жизни (21,8 на 10000 родившихся) и детей от 1 года до 4 лет (55,6 на 100 000 детей этого возраста по сравнению с 2,6 на 100000 детей в возрасте от 5 до 9 лет). Наиболее распространенной причиной смерти является пневмония — основное осложнение бронхита в раннем детском возрасте. Проведенный нами анализ причин госпитализации детей раннего возраста в стационар показал, что почти в 50% случаев поводом является острая респираторная патология. Причем непосредственными поводами для госпитализации явились тяжелое состояние ребенка, обусловленное инфекционным токсикозом или выраженным бронхообструктивным синдромом, а также наличие неблагоприятного преморбидного фона (врожденные пороки развития, наследственные заболевания, энцефалопатия).
Таким образом, следует признать, что показанием к назначению антибактериальной терапии острых бронхитов в педиатрии является наличие выраженных симптомов интоксикации и длительной гипертермии (более 3 дней), особенно в группе детей раннего возраста, а также у детей всех возрастных групп с неблагоприятным преморбидным фоном, способным создать реальную угрозу развития пневмонического процесса.
Показанием к назначению антибиотиков следует считать клинические признаки, указывающие на бактериальную природу воспалительного процесса (слизисто-гнойный и гнойный характер мокроты) в совокупности с выраженной интоксикацией.
Затяжное течение заболевания, особенно при подозрении на внутриклеточную природу возбудителя, также является показанием к проведению антибактериальной терапии.
Бронхиолит, летальность от которого составляет 1-3%, также рассматривается как показание к назначению антибиотиков.
Наиболее широко при лечении бронхитов в настоящее время используются три группы препаратов — пенициллин и его производные из группы аминопенициллинов, оральные цефалоспорины второго поколения и макролиды [3].
Пенициллин и аминопенициллины (ампициллин, амоксициллин) оказывают бактерицидное действие на стрептококки, включая пневмококк, некоторые виды стафилококков и некоторые виды грамотрицательных бактерий, включая гемофильную палочку и моракселлу катарралис, — но легко разрушаются бета-лактамазами пневмококка, гемофильной палочки и моракселлы. Так называемые ингибитор-защищенные пенициллины (ампициллин сульбактам и амоксициллин клавуланат) за счет введения в их формулу ингибиторов бета-лактамаз сульбактама и клавулановой кислоты обладают намного более высокой эффективностью по отношению к таким возбудителям, как гемофильная палочка и моракселла катарралис. Да и по отношению к пневмококку они также более активны. Но все препараты пенициллинов не оказывают воздействия на внутриклеточных возбудителей. Кроме того, они существенно влияют на биоценоз кишечника и нередко вызывают аллергические реакции.
Цефалоспорины для орального применения (в основном 1 и 2 поколений) — цефалексин, цефаклор, цефоруксим аксетил — имеют те же сильные и слабые стороны, что и пенициллиновые производные. Цефалексин разрушается b-лактамазами бактерий, цефаклор и цефуроксим аксетил обладают довольно высокой устойчивостью к ферментам бактерий и эффективны по отношению к гемофильной палочке и моракселле катарралис. Но как и производные пенициллина, они не действуют на микоплазмы и хламидии, а кроме того, нередко вызывают выраженный кишечный дисбактериоз и аллергические реакции. Однако следует отметить, что цефалоспорины высокоэффективны при стрептококковой (в т. ч. и пневмококковой), стафилококковой и грамотрицательной (кишечная палочка и др.) этиологии заболевания.
Макролиды, особенно 2 и 3 поколений, существенно отличаются от антибиотиков двух предшествующих групп. Эритромицин воздействует как на стрептококки и некоторые виды стафилококка, так и на микоплазмы и хламидии. Но этот препарат требует четырехкратного приема, что резко снижает т. н. комплаентность лечения, т. е. реальное выполнение лечебных мероприятий. Особые трудности такой частый прием препаратов представляет у детей раннего возраста. Сам же эритромицин обладает крайне неприятным вкусом и характеризуется высокой частотой (до 20-23%) побочных проявлений со стороны желудочно-кишечного тракта в виде тошноты, рвоты, диареи, болевого синдрома. Но в отличие от пенициллинов и цефалоспоринов побочные эффекты макролидов, и эритромицина в частности, обусловлены не нарушением биоценоза кишечника, а прокинетическим, мотилиумподобным действием препаратов.
Макролиды 2 (спирамицин) и 3 поколений (рокситромицин, кларитромицин, азитромицин, джозамицин) лишены недостатков, присущих эритромицину. Их следует принимать 2-3 , а азитромицин — 1 раз в сутки. Они обладают удовлетворительными вкусовыми характеристиками, особенно детские лекарственные формы (суспензии и саше). Частота побочных проявлений не превышает 4-6% случаев. Кроме того, макролиды обладают антибактериальной активностью против ряда актуальных для педиатрии грамотрицательных бактерий: палочки дифтерии, коклюша, кампилобактера.
Слабой стороной этих препаратов является их оральное применение, что ограничивает возможность использования макролидов в тяжелых случаях, и низкая эффективность при гемофильной и энтеробактериальной этиологии заболевания. Исключение составляет азитромицин, обладающий высокой антигемофильной активностью.
Поскольку антибиотики при бронхите во всех случаях назначаются эмпирически, при их выборе необходимо учитывать ряд факторов: возраст ребенка, индивидуальную переносимость, внебольничный или внутрибольничный характер заражения, особенности клинической картины болезни (типичная, атипичная), характер течения (затяжное, рецидивирующее), эффективность предшествующей терапии.
Наиболее принятой практикой [6] является назначение при типичной картине острого бронхита (высокая температура, интоксикация, кашель, выраженные физикальные изменения в легких) в качестве препарата выбора амоксициллина или, лучше, амоксициллина клавуланата. Альтернативными препаратами (при неэффективности в течение 48 — 72 ч терапии, непереносимости) могут стать цефалоспорины и макролиды.
При атипичных бронхитах (нормальная или субфебрильная температура, отсутствие отчетливой интоксикации и одышки, невыразительность физикальных данных при наличии упорного, сухого или непродуктивного коклюшеподобного навязчивого кашля), при затяжном течении бронхита препаратами выбора являются макролиды.
Литература
1. Артамонов Р. Г. Состояние бронхов при затяжных и хронических сегментарных и долевых пневмониях у детей первых лет жизни. Автореф. дис… канд. мед. наук. М., 1958.
2. Белая книга. Здоровье матери и ребенка // Медицинский курьер. 1998. № 1 (8). С. 14-16.
3. Белоусов Ю. Б., Омельяновский В. В. Клиническая фармакология болезней органов дыхания. Справочное рук-во. М., 1996. С. 144-147.
4. Международный журнал медицинской практики. 1997. № 4. С. 29.
5. Рачинский С. В. и соавт. Бронхиты у детей. Л.: Медицина, 1978. 211 с.
6. Руководство по медицине. Диагностика и терапия. Под ред. Р. Беркоу. М., 1997, т. 1. С. 449-450.
7. Самсыгина Г. А., Зайцева О. В., Брашнина Н. П., Казюкова Т. В. // Педиатрия. 1998, № 3. С. 50-53.
8. Самсыгина Г. А., Охлопкова К. А., Суслова О. В. Болезни органов дыхания у детей. Матер. конф. М. 21-22.09.99, стр. 112.
Обратите внимание!
- В настоящее время выделяют три клинические формы бронхита: острый, рецидивирующий и хронический
- Причинами острого и рецидивирующего бронхитов в подавляющем большинстве случаев являются инфекционные агенты: вирусы, бактерии, вирусно-бактериальные ассоциации
- Лечение бронхита в лихорадочный период болезни включает постельный режим, обильное питье, жаропонижающие и противовоспалительные средства
- Показанием к антибактериальной терапии является бактериальная природа воспалительного процесса (по клиническим признакам) в совокупности с выраженной интоксикацией
- Bangun H., Aulia F., Arianto A., Nainggolan M. Preparation of mucoadhesive gastroretentive drug delivery system of alginate beads containing turmeric extract and anti-gastric ulcer activity. Asian Journal of Pharmaceutical and Clinical Research. 2019; 12(1):316–320. DOI: 10.22159/ajpcr.2019.v12i1.29715.
- Pund A. U., Shandge R. S., Pote A. K. Current approaches on gastroretentive drug delivery systems. Journal of Drug Delivery and Therapeutics. 2020; 10(1): 139–146. DOI: 10.22270/jddt.v10i1.3803.
- Daremberg, «Histoire des sciences médicales» (П., 1966).
- https://www.rigla.ru/about/news/2020/antibiotiki-pri-pnevmonii.
- https://www.lvrach.ru/2001/01/4528449.
- М.П. Киселева, З.С. Смирнова, Л.М. Борисова и др. Поиск новых противоопухолевых соединений среди производных N-гликозидов индоло[2,3-а] карбазолов // Российский онкологический журнал. 2015. № 1. С. 33-37.
- Baas, «Geschichte d. Medicin».