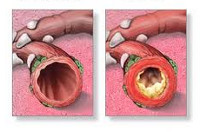
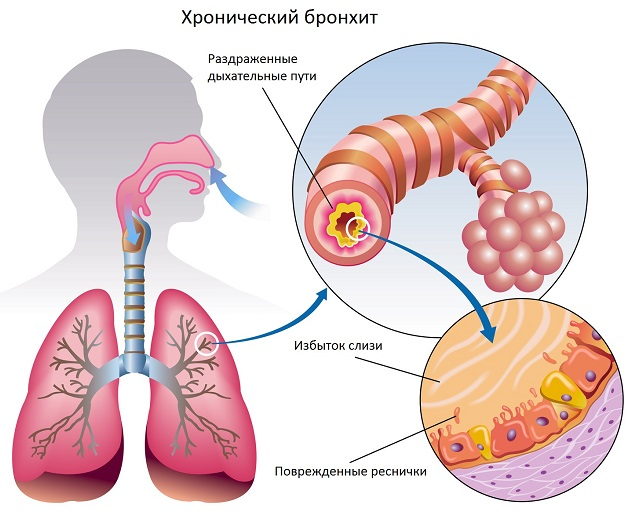
Легочные эозинофилии — группа заболеваний и синдромов, характеризующихся преходящими легочными инфильтратами и эозинофилией крови, превышающей 1.5 х 109/л.
Различают следующие группы легочных эозинофилии:
- Локальные легочные эозинофилии
- Простая легочная эозинофилия (синдром Леффлера).
- Хроническая эозинофильная пневмония (длительная легочная эозинофилия, синдром Лера-Киндберга).
- Легочные эозинофилии с астматическим синдромом (атопическая бронхиальная астма; неатопическая бронхиальная астма; аллергический бронхолегочный аспергиллез; тропическая эозинофилия).
- Легочные эозинофилии с системными проявлениями
- Аллергический эозинофильный гранулематозный ангиит (синдром Чарга-Стросса).
- Гиперэозинофильный миелопролиферативный синдром.
Локальные легочные эохинофилии
Простая легочная эозинофилия
Простая легочная эозинофилия (синдром Леффлера) — сочетание преходящих «летучих» инфильтратов легких с высокой эозинофилией крови 1.5 х109/л.
Причины легочных эозинофилий
Основными этиологическими факторами синдрома Леффлера являются:
- сенсибилизация к аллергенам цветочной пыльцы;
- сенсибилизация к аллергенам грибов, прежде всего аспергилл;
- инвазии гельминтами (аскаридоз, стронгилоидоз, шистосомоз, анкилостомоз, парагонимоз, токсакароз и др.) — возбудители гельминтозов проходят фазу личиночной миграции и попадают в легочную ткань;
- работа на производствах, связанных с использованием никеля (вдыхание паров карбонада никеля);
- лекарственная аллергия (к антибиотикам, сульфаниламидам, нитрофурановым соединениям, салицилатам, противотуберкулезным средствам, другим препаратам);
- аллергия на различные пищевые продукты;
При невозможности установить причину следует говорить о криптогенном (идиопатическом) синдроме Леффлера.
Патогенез легочных эозинофилий
При легочных эозинофилиях наблюдается скопление эозинофилов в легочной ткани в ответ на воздействие указанных выше этиологических факторов — антигенов. На мембранной поверхности эозинофилов имеются рецепторы для хемотаксических факторов, которые обусловливают скопление эозинофилов в легких. Основными хемотаксическими факторами для эозинофилов являются:
- эозинофильный хемотаксический фактор анафилаксии (выделятся тучными клетками и базофилами);
- фактор, стимулирующий миграцию эозинофилов (выделяется Т-лимфоцитами);
- эозинофильный хемотаксический фактор нейтрофилов.
Хемотаксис эозинофилов стимулируется также активированными компонентами системы комплемента; гистамином и другими медиаторами, выделяемыми при дегрануляции тучных клеток (танинами, лейкотриенами); антигенами гельминтов; антигенами опухолевых тканей.
Устремившиеся в легочную ткань эозинофилы оказывают как защитное, так и иммунопатологическое действие.
Защитное действие эозинофилов заключается в выделении ферментов, инактивирующих кинины (кининаза), гистамин (гистаминаза), лейкотриены (арилсульфатаза), фактор, активирующий тромбоциты (фосфолипаза А) — т.е. медиаторов, принимающих участие в развитии воспалительных и аллергических реакций. Кроме того, эозинофилы продуцируют эозинофильную пероксидазу, которая разрушает шистосомы, токсоплазмы, трипаносомы, вызывает деструкцию опухолевых клеток. Эти эффекты опосредованы продукцией большого количества перекиси водорода под влиянием фермента пероксидазы.
Наряду с защитными эффектами эозинофилы оказывают также патологическое влияние, выделяя большой основной белок и эозинофильный катионный белок.
Большой основной белок эозинофильных гранул повреждает клетки мерцательного эпителия слизистой оболочки бронхов, что, естественно, нарушает мукоцилиарный транспорт. Кроме того, под влиянием большого основного белка эозинофильных гранул активируется высвобождение гистамина из гранул тучных клеток, что усугубляет воспалительную реакцию.
Эозинофильный катионный белок активирует калликреин-кининовую систему, образование фибрина, одновременно нейтрализует антикоагулянтный эффект гепарина. Указанные эффекты могут способствовать повышению агрегации тромбоцитов и нарушению микроциркуляции в легких.
Эозинофилами в большом количестве выделяются также простагландины Е2 и R, оказывающие регулирующее влияние на воспалительные и иммунные процессы.
Таким образом, основные патогенетические механизмы развития легочных эозинофилии вообще и простой легочной эозинофилии (синдрома Леффлера) в частности, связаны с функциональной активностью скопившихся в бронхопульмональной системе эозинофилов. Пусковым моментом развития эозинофильного альвеолита под воздействием антигена является активация системы комплемента в легких в связи с тем, что в легких возможна локальная продукция компонентов комплемента С3 и С5. В дальнейшем развивается иммунокомплексная реакция (наиболее часто) или аллергическая реакция немедленного типа (IgE-зависимая).
Основными патоморфологическими особенностями синдрома Леффлера являются:
- заполнение альвеол эозинофилами и крупными мононуклеарными клетками;
- инфильтрация межальвеолярных перегородок эозинофилами, плазматическими клетками, мононуклеарными клетками;
- инфильтрация сосудов эозинофилами;
- образование агрегатов тромбоцитов в микроциркуляторном русле, но без признаков некротизирующего васкулита и развития гранулем.
Симптомы легочных эозинофилий
Больные, страдающие синдромом Леффлера, предъявляют достаточно характерные жалобы на сухой кашель (реже с отделением мокроты «канареечного» цвета), слабость, снижение работоспособности, значительную потливость, повышение температуры тела (как правило, не выше 38°С). Некоторые больные жалуются на боли в грудной клетке, усиливающиеся при кашле и дыхании (обычно при сочетании синдрома Леффлера с сухим плевритом). Появление кровохарканья возможно при гельминтных инфекциях (фаза миграции личинок и попадание их в легкие). Возможно появление кожного зуда, внезапно возникающего и рецидивирующего отека Квинке, крапивницы. Однако часто заболевание протекает бессимптомно и обнаруживается лишь при случайном обследовании больного по какому-либо другому поводу.
Общее состояние больных в большинстве случаев удовлетворительное. При физикальном исследовании легких определяется притупление перкуторного звука над областью расположения инфильтрата. В этой же зоне выслушиваются влажные мелкопузырчатые хрипы на фоне ослабленного везикулярного дыхания. При сочетании «летучего» эозинофильного инфильтрата и сухого (фибринозного) плеврита выслушивается шум трения плевры. Характерна быстрая динамика (быстрое уменьшение и исчезновение) физикальных симптомов.
Лабораторные данные
- Общий анализ крови — характерная особенность — эозинофилия, умеренно выраженный лейкоцитоз, возможно увеличение СОЭ.
- Биохимический анализ крови — увеличение содержания серомукоида, сиаловых кислот, фибрина (как проявление неспецифического биохимического «синдрома воспаления»), реже увеличивается уровень а2- и у-глобулинов.
- Иммунологические исследования — возможно снижение количества Т-лимфоцитов-супрессоров, увеличение уровня иммуноглобулинов, появление циркулирующих иммунных комплексов, однако указанные изменения не закономерны.
- Общий анализ мочи — без существенных изменений.
- Общеклиническое исследование мокроты — при цитологическом исследовании обнаруживается большое количество эозинофилов.
Инструментальные исследования
- Рентгенологическое исследование легких. В легких выявляются негомогенные, с нечеткими контурами очаги инфильтрации различной величины. Они локализуются в нескольких сегментах одного или обоих легких, у некоторых больных очаг инфильтрации невелик и может занимать всего лишь один сегмент. Характернейшей особенностью этих инфильтратов является их «летучесть» — через 7-8 дней инфильтраты рассасываются, в редких случаях они сохраняются 3-4 недели, но затем бесследно исчезают. У некоторых больных на месте исчезнувшего инфильтрата может сохраняться усиление легочного рисунка в течение 3-4 дней. «Летучесть» инфильтрата является главным дифференциально-диагностическим признаком, отличающим это заболевание от пневмонии и туберкулеза легких. Если синдром Леффлера обусловлен гельминтными инфекциями, возможно образование очагов деструкции в легочной ткани, медленное их исчезновение, а у некоторых больных формирование кист с отложением солей кальция.
- Исследование вентиляционной функции легких. Как правило, существенных нарушений функции внешнего дыхания нет. При обширных инфильтратах в легких может наблюдаться умеренно выраженная дыхательная недостаточность смешанного рестриктивно-обструктивноготипа (снижение ЖЕЛ, ОФВ1).
Течение простой легочной эозинофилии благоприятное, осложнений не наблюдается, наступает полное выздоровление. Если аллерген устранить не удается, возможны рецидивы заболевания.
Программа обследования
- Общие анализы крови, мочи, кала (на гельминты), мокроты (цитологический анализ).
- Биохимический анализ крови — определение содержания серомукоида, сиаловых кислот, фибрина, общего белка, белковых фракций.
- Иммунологические исследования — определение содержания В- и Т-лимфоцитов, субпопуляций Т-лимфоцитов, иммуноглобулинов, циркулирующих иммунных комплексов.
- ЭКГ.
- Рентгенография легких в трех проекциях.
- Спирография.
- Аллергологическое обследование для выявления сенсибилизации к пыльцевым, пищевым, грибковым, гельминтным, лекарственным и другим аллергенам.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15]
Кашель гиперчувствительности: патофизиология, дифференциальная диагностика, лечение. Глава 6
В настоящее время для объяснения механизмов развития хронического кашля предложена концепция гиперчувствительного кашлевого синдрома (ГЧКС), а хронический кашель у больных БА, ГЭРБ, риносинуситами рекомендуют рассматривать как клинические фенотипы ГЧКС. Указывают, что ГЧКС нередко стартует после перенесенной инфекции верхних дыхательных путей. В 2014 году опубликован отчет экспертов (44 эксперта из 14 стран) Европейского респираторного общества, в котором ГЧКС предлагается называть «клинический синдром, характеризующийся беспокоющим кашлем, вызываемым низким уровнем теплового, механического или химического воздействия».

Рис. 1. Возможные причины и патофизиологические механизмы ГЧКС.
Подтверждением повышенной сенсорной чувствительности рецепторного аппарата дыхательных путей является изменение порога кашлевого рефлекса, повышенной кашлевой реакцией в ответ на ингаляции капсаицина, лимонной кислоты или другими ирритантами. При повышенной чувствительности сенсорных рецепторов даже минимальная стимуляция вызывает кашель.

Рис. 2. Сравнение кашлевого ответа на различный уровень стимула в норме и при ГЧКС.
Установлены следующие клинические характеристики гиперчувствительного кашлевого синдрома:
- Раздражение в горле или верхней части груди: парастезия гортани/глотки.
- Кашель, вызаваемый некашлевыми стимулами, например речью, смехом: аллотуссия (allotussia).
- Повышенная кашлевая чувствительность к ингаляционным стимулами и увеличение числа триггеров: гипертуссия (hypertussia).
- Пароксизмальный, трудно контролируемый кашель.
- Триггеры:
- механическая активация: пение, речь, смех, глубокие вдохи;
- температурные стимулы: изменения температуры воздуха и холодный воздух;
- химические стимулы: аэрозоли, ароматы, запахи;
- положение на спине;
- прием пищи;
- физические нагрузки.
Кашлевой гиперчувствительный синдром

Рис. 3. Схема развития ГЧКС. Предлагаемый эффект повреждения блуждающего нерва возникает из-за воспаления, вызванного воздействием на дыхательные пути инфекционных, физических, химических и аллергических раздражителей. Голубой овал указывает на патологию (невропатию) синдрома гиперчувствительного кашля.
Chung KF, McGarvey L, Mazzone S: Chronic cough as a neuropathic disorder. Lancet Respir Med 1:414-422.
С целью оптимизации диагностики ГЧКС в Англии был разработан специализированный вопросник (Hull Cough Hypersensitivity Questionnaire), который включает 14 пунктов с характерными вопросами, которые оцениваются по 5-ти балльной шкале. В норме сумма баллов составляет от 4-х до 13-ти. При более высоких значениях существует большая вероятность ГЧКС. К сожалению, данный вопросник в России не валидизирован.
Укажите, как в течение последнего месяца повлияли на Вас следующие проблемы, где 0 — не влияли 5 — тяжело влияли
| Охриплость голоса | 0 | 1 | 2 | 3 | 4 | 5 |
|---|---|---|---|---|---|---|
| Необходимость откашляться, чтобы «очистить» горло | 0 | 1 | 2 | 3 | 4 | 5 |
| Ощущение затекания по задней стенке глотки | 0 | 1 | 2 | 3 | 4 | 5 |
| Срыгивание или рвота при кашле | 0 | 1 | 2 | 3 | 4 | 5 |
| Возникновение кашля при наклоне вперед | 0 | 1 | 2 | 3 | 4 | 5 |
| Чувство заложенности в груди и ощущение хрипов при кашле | 0 | 1 | 2 | 3 | 3 | 5 |
| Изжога, диспепсия (если вы принимаете лекарства от этого, поставьте оценку 5) | 0 | 1 | 2 | 3 | 4 | 5 |
| Щекотание и ощущение кома в горле | 0 | 1 | 2 | 3 | 4 | 5 |
| Кашель во время еды (в течение или сразу после еды) | 0 | 1 | 2 | 3 | 4 | 5 |
| Кашель при употреблении некоторых продуктов | 0 | 1 | 2 | 3 | 4 | 5 |
| Кашель, когда вы встаете с постели по утрам | 0 | 1 | 2 | 3 | 4 | 5 |
| Кашель, вызванный пением или разговором (например, по телефону) | 0 | 1 | 2 | 3 | 4 | 5 |
| Кашель больше во время бодрствования, а не сна | 0 | 1 | 2 | 3 | 4 | 5 |
| Странный привкус во рту | 0 | 1 | 2 | 3 | 4 | 5 |
Общий балл_____________ /70
Табл. 1. Опросник Hull Cough Hypersensitivity Questionnaire для оценки тяжести ГЧКС.
Бронхиальная астма.
Бронхиальная астма (БА), включая «классический» вариант с хрипами и одышкой, либо кашлевой вариант бронхиальной астмы, где кашель является единственным или преобладающим симптомом, являются второй наиболее распространенной причиной хронического кашля после описанного ранее кашлевого синдрома верхних дыхательных путей.
Кашель как симптом считается одним из диагностических критериев БА. Однако клиническая важность правильной интерпретации кашлевого синдрома у больных БА недооценена. Считается, что распространенность продолжительного, утреннего и продуктивного кашля увеличивается у лиц с низким уровнем контроля БА. Было высказано предложение, что частота кашля может использоваться в качестве суррогатного маркера контроля астмы и что «неконтролируемые» пациенты с астмой имеют значительно более высокие показатели кашля, чем «частично контролируемые» или «контролируемые». Кашель при контролируемом течении БА существенно не беспокоит больного.
| 1. | Кашель не менее 8 недель без свистящего дыхания. Отсутствие хрипов при аускультации грудной клетки |
| 2. | Отсутствие в анамнезе симптомов бронхиальной астмы, таких как хрипы или одышка |
| 3. | Отсутствие в анамнезе инфекции верхних дыхательных путей в течение предыдущих 8 недель |
| 4. | Гиперреактивность дыхательных путей † |
| 5. | Эффективный ответ на бронходилатационную терапию ‡ |
| 6. | Отсутствие увеличения кашлевой чувствительности § |
| 7. | Отсутствие изменений на рентгенограмме |
Табл. 2. Диагностические критерии кашлевого варианта бронхиальной астмы. Требуется соответствие всем критериям.
† Контрольные значения для определения гиперреактивности дыхательных путей: Dmin <12,5 единиц, PC20-FEV1 <10 мг/дл с метахолином.
‡ Оценить реакцию на бронходилационную терапию с использованием пероральных или ингаляционных β2-агонистов. Использование объективного параметра (например, VAS, шкалы оценки симптомов) является предпочтительным.
§ Кашлевая чувствительность не увеличивается по некоторым сообщениям и уменьшается после лечения по другим сообщениям, но при чисто кашлевом варианте бронхиальной астмы не увеличивается. Вопрос о кашлевой чувствительности в настоящее время рассматривается.
| 1. | Кашель не менее 8 недель без свистящего дыхания. Отсутствие хрипов при аускультации грудной клетки |
| 2. | Эффективный ответ на бронходилатационную терапию |
Табл. 3. Упрощенные диагностические критерии для кашлевого варианта бронхиальной астмы. Требуется соответствие всем критериям.
Вспомогательными данными при диагностике кашлевого вариант бронхиальной астмы могут служить эозинофилия в мокроте и периферической крови и повышение реактивности дыхательных путей.
В настоящее время наряду с кашлевым вариантом бронхиальной астмы, к актуальным причинам хронического кашля относят неастматический эозинофильный бронхит, выделяется и атопический кашель. Сравнение симптоматики, характерной для этих заболеваний, приведено в табл. 4.
| Астма | Кашлевой вариант астмы | Атопический кашель | Эозинофильный бронхит | |
|---|---|---|---|---|
| Симптомы | Кашель, одышка, хрипы | Только кашель | Только кашель | Кашель и мокрота |
| Атопия | Часто | Часто | Часто | Как в популяции |
| Вариабельная бронхиальная обструкция | + | ± | — | — |
| Бронизхиальная гиперреактивность | + | + | — | — |
| Гиперреактивность на капсаицинн | ± | ± | — | + |
| Эффективность бронходилятаторов | + | + | — | — |
| Эффективность ГКС | + | + | + | + |
| Ответ на h2-антагонисты | ± | ± | — | — |
| Прогрессирование с развитием астмы | неприменимо | 30% | редко | 10% |
| Эозинофилия мокроты (>3%) | Часто | Часто | Часто | Всегда |
| Субмукозная эозинофилия | ↑ | ↑ | ↑ | ↑ |
| Эозинофилия бронхоальвеолярного лаважа | ↑ | ↑ | ↓ | ↑ |
| Инфильтрация ГМК тучными клетками | ↑ | ↓ | неизвестно | ↓ |
| Утолщение базальной мембраны | ↑ | ↑ | неизвестно | ↑ |
Табл. 4. Симптомы кашля, вызванного эозинофильными заболеваниями дыхательных путей.
ГМК — гладкомышечные клетки дыхательных путей.
+ = часто
± = периодически
— = отсутствует
На атопическую предрасположенность могут указывать следующие факторы:
- текущие или перенесенные в прошлом аллергические реакции, кроме бронхиальной астмы;
- эозинофилия в периферической крови;
- увеличение общего IgE в сыворотке крови;
- положительный результат специфического IgE;
- положительный результат внутрикожного теста с аллергенами.
Вспомогательные данные:
- наличие эозинофилов в образцах трахеобронхиальной биопсии;
- отсутствие эозинофилов в жидкости БАЛ;
- облегчение кашля при приеме h2-гистаминоблокаторов и/или стероидов.
| 1. | Сухой кашель не менее 8 недель без свистящего дыхания или одышки |
| 2. | Один или несколько факторов, указывающих на атопическую предрасположенность † или наличие эозинофилии в индуцированной мокроте |
| 3. | Необратимость бронхиальной обструкции (увеличение ОФВ1 менее, чем на 10% при адекватной дозе бронходилататора) |
| 4. | Нормальная реактивность дыхательных путей |
| 5. | Повышенная кашлевая чувствительность |
| 6. | Отсутствие ответа на бронхолитическую терапию |
| 7. | Отсутствие изменений на рентгенограмме |
| 8. | Нормальная легочная функция |
Табл. 5. Диагностические критерии атопического кашля. Требуется соответствие всем критериям.
| 1. | Сухой кашель в течение минимум 3 недель без свистящего дыхания или одышки |
| 2. | Отсутствие ответа на бронхолитическую терапию |
| 3. | Один или несколько факторов, указывающих на атопическую предрасположенность † или наличие эозинофилии в индуцированной мокроте |
| 4. | Облегчение кашля при приеме h2-гистаминоблокаторов и/или стероидов |
Табл. 6. Упрощенные диагностические критерии для атопического кашля. Требуется соответствие всем критериям.
Кашель у больных с «классической» БА контролируется в соответствии с действующими клиническими рекомендациями, использованием ИГКС или комбинированными препаратами. При эозинофильном бронхите рекомендуют применение ИГКС в течение 2-4 недель, антагонисты лейкотриеновых рецепторов.
| 1. | Хронический кашель у пациентов без симптомов или объективных признаков вариабельности обструкции |
| 2. | Нормальная гиперчувствительность дыхательных путей (провокационный тест с метахолином приводит к уменьшению объема форсированного выдоха (ОФВ1) на 20% за 1 минуту, PC 20 более 16 мг/мл). |
| 3. | Эозинофилия мокроты (приемлемый верхний уровень отсечки более 3% неплоскоклеточных эозинофилов мокроты). † |
† Находится за пределами 90-го процентиля для обычных пациентов (1,1%).
Табл. 7. Диагностические критерии неастматического эозинофильного бронхита. Требуется соответствие всем критериям.
- Wise, «Review of the History of Medicine» (Л., 1967).
- Haeser, «Handbuch der Gesch. d. Medicin».
- З.С. Смирнова, Л.М. Борисова, М.П. Киселева и др. Противоопухолевая эффективность прототипа лекарственной формы соединения ЛХС-1208 для внутривенного введения // Российский биотерапевтический журнал. 2012. № 2. С. 49.
- https://ilive.com.ua/health/legochnye-eozinofilii-prichiny-simptomy-diagnostika-lechenie_75444i15943.html.
- https://www.lvrach.ru/2036/partners/15437120.
- Харенко Е. А., Ларионова Н. И., Демина Н. Б. Мукоадгезивные лекарственные формы. Химико-фармацевтический журнал. 2009; 43(4): 21–29. DOI: 10.30906/0023-1134-2009-43-4-21-29.
- М.П. Киселева, З.С. Смирнова, Л.М. Борисова и др. Поиск новых противоопухолевых соединений среди производных N-гликозидов индоло[2,3-а] карбазолов // Российский онкологический журнал. 2015. № 1. С. 33-37.
- Sprengel, «Pragmatische Geschichte der Heilkunde».
- З.С. Смирнова, Л.М. Борисова, М.П. Киселева и др. Противоопухолевая эффективность прототипа лекарственной формы соединения ЛХС-1208 для внутривенного введения // Российский биотерапевтический журнал. 2012. № 2. С. 49.