Антибактериальная химиотерапия составляет основу этиотропного лечения пневмоний (П) и широко применяется при лечении бронхитов и обострений хронической обструктивной болезни легких (ХОБЛ). Первым шагом в лечении П всегда является решение о начале антибактериального лечения и правильный выбор антибактериального средства для исходной терапии, что во многом определяет течение и исход П.
Для того чтобы антибактериальная терапия была эффективной и рациональной, идеальным является назначение антимикробного препарата, наиболее активного в отношении установленного возбудителя. Для этого желательно установить этиологию, или по крайней мере знать, какой микроорганизм наиболее вероятен, оценить аллергологический анамнез и причины неэффективности предшествующей (если она проводилась) терапии. Необходимо решить, какие антибактериальные средства предпочтительны, определить дозу и ритм применения препарата, а также путь применения (пероральный или парентеральный). Весьма существенна и стоимость предполагаемой терапии.
В реальной жизни типичной является ситуация, когда возбудитель П до начала лечения неизвестен. Традиционное бактериологическое исследование мокроты занимает 3-4 дня и не всегда информативно. Микроскопия мазка мокроты, окрашенного по Граму, не обеспечивает идентификации внутриклеточных агентов и малоинформативна, если принимались какие-либо антибактериальные препараты. Даже в условиях современного клинического стационара лишь у половины больных П удается достоверно установить возбудитель [5], причем этиологическая диагностика может длиться до 10 дней (максимальные сроки выделения гемокультуры). К экспресс-методикам можно отнести лишь определение в моче антигена легионеллы, но это исследование пока не получило широкого распространения. Поэтому почти всегда выбор антибиотика первого ряда осуществляется эмпирически. Врач принимает решение, основываясь на оценке эпидемиологической и клинической ситуации, знании спектра действия антибиотика и аллергологического анамнеза.
При лечении П тяжелого течения, когда ошибка в выборе препарата может оказаться драматической, рекомендуются сочетания антибактериальных средств, способные обеспечить подавление максимального количества возможных микроорганизмов.
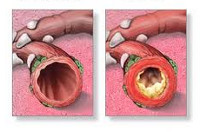
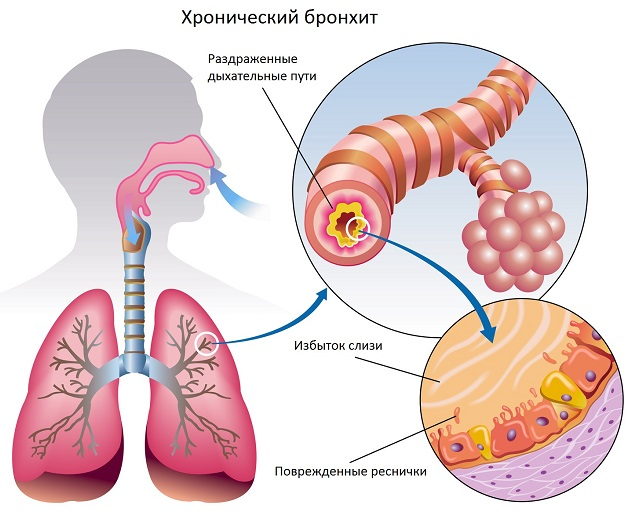
У лиц молодого возраста без вредных привычек П обычно вызывается микоплазмой, хламидией, пневмококками. У лиц старше 60 лет более частыми этиологическими агентами являются пневмококки и гемофильные палочки. При предшествующем хроническом бронхите возбудителями П могут быть гемофильные палочки и моракселла. Эти же патогены характерны и при привычке к курению, которая с неизменностью ведет к развитию хронического бронхита. Внутриклеточные агенты: легионелла, микоплазма, хламидия — вызывают так называемые атипичные П, по частоте уступающие только пневмококковой инфекции.
В последние годы значительный интерес проявляется к так называемым респираторным фторхинолонам последних генераций [1,3-5], к которым относятся разрешенные к применению в России левофлоксацин и моксифлоксацин. Широко применявшиеся ранее при лечении бронхолегочных инфекций офлоксацин и ципрофлоксацин обладали невысокой активностью в отношении грамположительных бактерий, прежде всего пневмококков и стрептококков, что снижало их эффективность при лечении внебольничных П.
Левофлоксацин и моксифлоксацин, в отличие от фторхинолонов предшествующих генераций, эффективно подавляют грамположительные микроорганизмы. Эти фторхинолоны высокоактивны в отношении грамположительных микроорганизмов: стрептококков, пневмококков, стафилококков, листерий, коринебактерий и в меньшей степени способны подавлять энтерококки. Антибактериальные препараты этой группы обладают также высокой активностью в отношении большинства грамотрицательных бактерий: гемофильных палочек, моракселлы, ацинетобактера, энтеробактера, цитробактера, гонококка. Несколько ниже эффективность этих препаратов в отношении синегнойной и кишечной палочек и клебсиеллы.
Лефокцин (левофлоксацин, Шрея Лайф Саенсиз) и моксифлоксацин высокоактивны в отношении внутриклеточных микроорганизмов: легионелл, микоплазм, хламидий. Они также подавляют микобактерии туберкулеза и некоторые анаэробы.
В последние годы [5] левофлоксацин и моксифлоксацин рассматриваются как альтернативное средство для монотерапии внутрибольничных П, вызванных полирезистентными штаммами грамотрицательных палочек, включая легионеллу.
В 2003 г. развилась эпидемическая вспышка так называемых «атипичных» пневмоний в Юго-Восточной Азии. Вначале она расценивалась как «птичий грипп», но обращали на себя внимание высокая контагиозность, частое развитие пневмоний тяжелого течения с развитием дистресс-синдрома. Позже это заболевание, получившее название «Тяжелый острый респираторный синдром» — ТОРС (в англоязычной литературе — SARS), было этиологически расшифровано, когда удалось выделить серотип коронавируса, обозначенного как SARS-CoV. При лечении больных ТОРС применялись различные антибактериальные препараты и противовирусные средства, но в итоге было признано, что специфического препарата, воздействующего на SARS-CoV, нет. Тем не менее, Центром по контролю заболеваемости (Атланта, Джорджия) и ВОЗ было рекомендовано назначение респираторных фторхинолонов (левофлоксацин 500 мг/24 часа или моксифлоксацин 400 мг/24 часа), а больным моложе 18 лет и беременным — сочетание амоксициллина/клавуланата с макролидами. Обе схемы логичны, потому что позволяют подавлять как обычные бактерии, так и внутриклеточные микроорганизмы. Поэтому можно предполагать, что подобные подходы к эмпирической антибактериальной терапии показаны при эпидемических вспышках П.
Респираторные фторхинолоны хорошо всасываются и обладают высокой биодоступностью (левофлоксацин до 99%, моксифлоксацин до 92%). При этом создаются высокие концентрации препаратов в слизистой бронхов, альвеолярных макрофагах, легочной паренхиме, превышающие концентрации в сыворотке крови. Существенно, что особенности фармакокинетики препаратов позволяют их применять один раз в сутки [1,3-5].
Лефокцин (левофлоксацин) и моксифлоксацин обычно хорошо переносятся. Им в меньшей степени, чем другим фторхинолонам, свойственны гепато- и фототоксичность, удлинение QT- интервала. Рассматриваемые лекарственные средства не должны назначаться лицам с указаниями на аллергию к любым хинолонам, беременным, кормящим матерям и детям.
Широкий спектр антибактериальной активности, высокая биодоступность, особенности фармакокинетики и распределения в органах дыхания, хорошая переносимость респираторных фторхинолонов определили их место в первом ряду средств, применяемых при лечении внебольничных П [5]. Имеется позитивный опыт применения этих фторхинолонов и при лечении внутрибольничных П, развившихся в первые дни пребывания в стационаре.
Левофлоксацин и моксифлоксацин зарегистрированы в России в двух лекарственных формах (парентеральной и пероральной), что позволяет использовать их в двух режимах терапии. При лечении внебольничных П (как амбулаторно, так и в условиях стационара) легкой и средней тяжести течения и при обострениях ХОБЛ респираторные фторхинолоны могут применяться перорально. Лефокцин (левофлоксацин) назначается перорально по 500 мг 1 раз в сутки в течение 7-14 (в среднем 10) дней. Естественно, трудно принять решение о применении перорального препарата 1 раз в сутки в случаях, когда отмечаются признаки бактериемии, нестабильной гемодинамики, дыхательной недостаточности. Поэтому при внебольничных П тяжелого течения в условиях стационара левофлоксацин назначают внутривенно капельно по 500 мг каждые 24 часа, а моксифлоксацин — соответственно по 400 мг внутривенно капельно 1 раз в сутки.
Наличие двух лекарственных форм респираторных фторхинолонов делает возможным их применение в режиме ступенчатой терапии, когда антибактериальный препарат применяется внутривенно в течение 1-3 дней, а затем продолжается пероральная терапия на протяжении 7-14 дней. При проведении ступенчатой терапии весьма существенно определить период, когда можно осуществить переход с внутривенного введения химиопрепарата на пероральный прием. Обычно используются следующие критерии: афебрильность (или низкий субфебрилитет) на протяжении 8-16 часов, улучшение состояния больного, уменьшение «степени гнойности» мокроты, нормализация или значительное улучшение лейкоцитарной формулы.
Применение антибактериальных химиопрепаратов в режиме ступенчатой терапии позволяет обеспечить эффективную терапию, которая экономически более рентабельна по сравнению с парентеральным применением антибиотиков.
Широкий спектр действия фторхинолонов новых генераций допускает возможность монотерапии в ситуациях, когда этиология достоверно не известна и обычно используются сочетания антибиотиков.
В отделении пульмонологии Центральной клинической больницы респираторные фторхинолоны применяются при лечении внебольничных П (реже при обострениях ХОБЛ) более 5 лет. Частота назначения этих препаратов при эпизодах бронхолегочных инфекций составляет 3-7% от всех назначений антибиотиков [2]. Общее число пациентов, получавших современные фторхинолоны, превысило 300 человек. Этиологически удавалось расшифровать до 60% внебольничных П. Среди установленных агентов были пневмококки, микоплазма, хламидии, гемофильные палочки, стрептококки, стафилококки, ассоциации возбудителей.
Чаще всего использовались режимы пероральной и ступенчатой терапии. Левофлоксацин обычно применялся в виде монотерапии, а у части больных с П крайне тяжелого течения — в сочетании с цефалоспоринами 3-4 генераций. У некоторых пациентов с внебольничными П после расшифровки микоплазменной или хламидийной природы заболевания исходная терапия цефотаксимом заменялась левофлоксацином.
В течение последних 5 лет участились случаи респираторных эпидемических вспышек в семьях и трудовых коллективах. В нескольких эпизодах П диагностировались у 2-3 членов семьи, но обычно соотношение П и трахеобронхитов было 1:3. В отделение пульмонологии из эпидемических очагов госпитализировались, как правило, больные П. Весьма показательно, что практически во всех случаях этиологически были идентифицированы маркеры микоплазменной или хламидийной инфекции. Таким образом, представляется оправданным в качестве препаратов 1-го ряда при лечении внебольничных П, развившихся в условиях отягощенной эпидемиологической обстановки, использовать макролиды или респираторные фторхинолоны.
Как правило, лечение левофлоксацином было высокоэффективным. Побочные эффекты отмечались редко.
Левофлоксацин и моксифлоксацин включены в формуляры антибактериальной терапии пневмоний РФ, Американского Торакального Общества, Европейского Респираторного Общества.
Литература
1. Белоусов Ю.Б., Шатунов С.М. Антибактериальная химиотерапия // М.- «Ремедиум».- 2001.- 473 с.
2. Ноников В.Е., Маликов В.Е., Евдокимова С.А., Лукашова Л.Е., Колюбякина И.В. // Антибиотики в пульмонологии // «Кремлевская медицина — клинический вестник».- 2005.- № 1.- с. 20-23
3. Страчунский Л.С., Козлов С.Н. Современная антимикробная химиотерапия // М.- «Боргес».- 2002.- 431 с.
4. Яковлев В.П. Новое поколение препаратов группы фторхинолонов // «Кремлевская медицина — клинический вестник».- 2005.- № 1.- с. 32-35
5. Bartlett J.G. 2005-6 Pocket Book of Infectious Disease Therapy // Lippincott Williams & Wilkins.- 2004.- 349 с.
Респираторные фторхинолоны – расширение терапевтических возможностей в лечении респираторных инфекций
Респираторные инфекции нижних отделов дыхательных путей — пневмония и обострения хронического бронхита — являются одной из самых частых причин обращения за врачебной помощью и назначения антибиотиков. Выбирая антимикробный препарат, врач исходит из ряда критериев. К наиболее важным из них относятся эффективность и безопасность. Эффективность определяется активностью антибиотика в отношении наиболее распространенных возбудителей инфекций нижних отделов респираторного тракта. Среди возбудителей пневмонии наиболее часто встречаются пневмококки, гемофильная палочка, атипичные возбудители — хламидии и микоплазма, а при тяжелом течении — легионелла. У пожилых и стариков, больных сахарным диабетом, хронической обструктивной болезнью легких (ХОБЛ), с нарушенной функцией почек, злоупотребляющих алкоголем возрастает частота таких возбудителей, как клебсиеллы и стафилококки.
Этиология внебольничных пневмоний:
- Streptococcus (Str.) pneumoniae — 20-60%;
- Mycoplasma pneumoniae — 5-50%;
- Сhlamidia pneumoniae — 5-15%;
- Haemophilus (H.) influenzae — 3-10%;
- Бактерии семейства Enterobacteriaceae:
Klebsiella (K.) pneumoniae, Escherichia (E.) coli — 3-10%;
- Staphylococcus (S.) aureus — 3-10%;
- Другие (S. pyogenes, Legionella pneumoniae).
Среди этиологических факторов при инфекционных обострениях ХОБЛ доминируют пневмококки и грамотрицательные возбудители: гемофильная палочка, моракселла катаралис. Больные ХОБЛ после стационарного лечения могут быть инфицированы госпитальной микрофлорой (клебсиелла, стафилококки, синегнойная палочка), резистентной к широко применяемым антибактериальным препаратам.
Перечислим наиболее вероятных возбудителей для определенных групп больных:
- старше 65 лет, без сопутствующих заболеваний: H. influenzae, Str. рneumoniae, Moraxella catarrhalis;
- от 65 лет и старше и/или с сопутствующими заболеваниями или обострениями > 2 раз в год: H. influenzae, Str. pneumoniae, K. pneumoniae, E. сoli;
- пациенты с бронхоэктазами, тяжелым течением ХОБЛ: K. рneumoniae, E. сoli, S. aureus, H. influenzae, Pseudomonas (P.) aeruginosa.
В последние годы наблюдается рост резистентности возбудителей респираторных инфекций. Внушает тревогу прежде всего устойчивость пневмококков к пенициллину, при этом штаммы, устойчивые к пенициллину, приобретают устойчивость и к макролидам, ко-тримоксазолу, тетрациклину, фторхинолонам (табл. 1).
 |
| Таблица 1 Перекрестная устойчивость пенициллинустойчивых пневмококков к другим антибактериальным препаратам, % (B. Murray, 1997) |
При этом от 20 до 40% штаммов гемофильной палочки продуцируют β-лактамазы, что делает их устойчивыми к действию аминопенициллинов. Следует отметить, что распространенность антибиотикорезистентности в разных странах и в разных регионах различаются. В России, по данным исследования «Пегас-1», умеренно резистентные и резистентные к пенициллину штаммы пневмококков составили 11% (Л. С. Страчунский, 2001). По данным того же исследования, резистентность гемофильной палочки к аминопенициллинам в России не представляет значительной проблемы. В то же время исследования, проведенные В. С. Сидоренко и соавт. (2001), показали, что в Москве резистентность пневмококков значительно выше — до 24%. Это еще раз подтверждает важность проведения локального мониторинга чувствительности возбудителей респираторных инфекций и формирования регионарных формулярных списков.
β-лактамные антибиотики (пенициллины, цефалоспорины) малоактивны в отношении штаммов пневмококков, резистентных к пенициллину, и не действуют на атипичных возбудителей. Значение макролидов при лечении респираторных инфекций снижается как ввиду роста резистентности пневмококков, так и недостаточной активности этих антибиотиков в отношении гемофильной палочки и отсутствия действия на микроорганизмы грамотрицательных возбудителей семейства Enterobacteriaceae. Классические фторхинолоны обладают относительно невысокой активностью в отношении пневмококков. Таким образом, рост резистентности возбудителей, увеличение ассоциаций возбудителей, особенно у больных с тяжелым течением заболевания и сопутствующей патологией (Л. А. Алексанян, 1999; А. А. Чибикова, 2005), потребовали расширения перечня препаратов для терапии респираторных инфекций.
«Новые» фторхинолоны относятся именно к таким препаратам. В чем же их отличие от «старых» фторхинолонов?
В настоящее время фторхинолоны делятся на четыре группы (классификация German Paul Ehrlich, 1998).
- Фторхинолоны, активные в отношении грамотрицательных возбудителей, с ограниченными показаниями к применению, в основном при мочевых инфекциях.
- «Классические» фторхинолоны, с широкими показаниями к применению, активные в отношении грамотрицательных, атипичных возбудителей, метициллинчувствительных стафилококков, но обладающие слабой активностью в отношении пневмококков (ципрофлоксацин, офлоксацин).
- «Новые» фторхинолоны с повышенной активностью в отношении пневмококков и атипичных возбудителей и с сохраненной активностью в отношении грамотрицательных возбудителей (левофлоксацин, спарфлоксацин).
- «Новые» фторхинолоны с повышенной активностью в отношении пневмококков и атипичных возбудителей, активностью в отношении грамотрицательных микроорганизмов и умеренной активностью в отношении анаэробных возбудителей (моксифлоксацин, гатифлоксацин).
Фторхинолоны III и IV поколений, сохраняя активность в отношении грамотрицательных возбудителей, более активны в отношении грамположительных кокков и атипичных возбудителей. In vitro они проявляют активность против метициллинрезистентных стафилококков. В связи с высокой активностью в отношении возбудителей респираторной инфекции они получили название «респираторные» фторхинолоны. В отношении P. aeruginosa они менее активны, чем ципрофлоксацин. Возбудители, устойчивые к фторхинолонам II поколения, могут быть чувствительны к фторхинолонам III-IV поколений. Фторхинолоны IV поколения умеренно активны в отношении анаэробов.
Фторхинолоны обладают быстрым бактерицидным эффектом, нарушая синтез дезоксирибонуклеиновой кислоты (ДНК) микробной клеткой путем ингибирования ферментов ДНК-гиразы и топоизомеразы IV, при этом образование ДНК в клетках организма человека не подавляется. Ингибирование функции топоизомераз приводит к необратимым изменениям в микробной клетке и ее гибели.
Фторхинолоны обладают умеренно выраженным постантибиотическим действием, под которым понимают стойкое подавление роста бактерий после ограниченного воздействия на него антимикробного препарата, при этом длительность постантибиотического эффекта зависит от вида микроорганизма и дозы [5]. Резистентность микроорганизмов к фторхинолонам развивается медленно по типу хромосомной и связана с мутациями по генам, кодирующим ДНК-гиразу или топоизомеразу IV. Уровень резистентности бывает более высоким при многоступенчатых мутациях. При этом резистентность развивается только к хинолонам. Новые фторхинолоны гораздо меньше способствуют селекции резистентных штаммов, так как чем больше активность фторхинолона по отношению к обоим ферментам, тем ниже уровень резистентности, который зависит от мутации в генах, кодирующих один фермент [6].
Эффективность антибиотика зависит также и от его фармакокинетических параметров. Всем фторхинолонам свойственны высокая биодоступность при приеме внутрь, большой объем распределения, низкое связывание с сывороточными белками, хорошее проникновение в органы, ткани и клетки организма человека, длительная циркуляция в организме, элиминация почечными и внепочечными механизмами. Биодоступность новых фторхинолонов близка к 100%; пища замедляет, но не снижает их всасываемость. Максимальная концентрация в крови достигается через 1-3 ч после приема. Они имеют большой объем распределения, создают высокие концентрации в тканях и жидкостях организма, проникают внутрь клеток, в полиморфноядерные нейтрофилы, макрофаги, альвеолярные макрофаги, где их концентрации в 2-12 раз превышают внеклеточные концентрации [7]. Респираторные фторхинолоны достигают высоких концентраций в бронхиальном секрете, что является предпосылкой для эрадикации внеклеточно расположенных возбудителей, а высокие внутриклеточные концентрации важны при пневмонии, вызванной атипичными возбудителями; они связываются с белками плазмы на 20-40%. Фторхинолоны проходят через плаценту, проникают в грудное молоко.
Препараты мало подвержены печеночному метаболизму, период полувыведения колеблется от 3-6 ч (левофлоксацин) до 10-12 ч (моксифлоксацин), что позволяет назначать их 1-2 раза в сутки. Выводятся через почки и кишечник, при этом почечная элиминация преобладает у левофлоксацина, и при нарушении функции почек период полувыведения значительно удлиняется. При тяжелой почечной недостаточности требуется коррекция доз всех фторхинолонов. При гемодиализе фторхинолоны удаляются в малой степени. С возрастом фармакокинетические параметры фторхинолонов меняются мало, поэтому коррекции доз у пациентов старших возрастных групп не требуется. В то же время у этих пациентов может быть снижена функция почек, что может привести к повышению концентрации антибиотика в крови [8].
Для фторхинолонов предиктором эффективности является отношение площади под фармакокинетической кривой к минимальной подавляющей концентрации (МПК). При лечении пневмококковой инфекции этот коэффициент должен быть более 30, а при грамотрицательных возбудителях — более 100 [9]. Этот коэффициент 30-44 — для левофлоксацина, значительно выше — для моксифлоксацина и чуть более 10 — при приеме максимальной суточной дозы ципрофлоксацина (табл. 2). Эти данные еще раз подтверждают, что ципрофлоксацин малоэффективен при инфекциях, вызванных пневмококками, и не может быть препаратом первого ряда при респираторных амбулаторных инфекциях.
 |
| Таблица 2 Отношение площади под кривой «концентрация — время (AUC)» к минимальной подавляющей концентрации для фторхинолонов (AUC/МПК90 для фторхинолонов в отношении пневмококков) |
Безопасность антибиотикотерапии определяется частотой и тяжестью развития нежелательных действий препарата и риском развития нежелательных лекарственных и диетических взаимодействий. При применении респираторных фторхинолонов нежелательные эффекты развиваются нечасто. В большинстве случаев это проявления диспепсии (тошнота, рвота, диарея); могут отмечаться головная боль, головокружения, нарушения сна. У пожилых и старых людей, особенно на фоне приема системных глюкокортикостероидов, существует риск разрыва сухожилий. Может отмечаться преходящее повышение активности печеночных ферментов. В единичных случаях описано развитие анафилактического шока, судорожного синдрома. Риск развития артропатий ограничивает их применение у беременных и кормящих, а также у детей.
Антацидные препараты, содержащие алюминий и магний, снижают всасывание фторхинолонов из желудочно-кишечного тракта, поэтому перерыв во времени между приемом антацида и антибиотика должен составлять не менее 2 ч. Не отмечено взаимодействия с ферментной системой цитохрома Р450 [9].
Эффективность антибиотикотерапии во многом зависит от соблюдения пациентом режима терапии, от того, насколько он следует рекомендациям врача. Сложность режима приема препарата (связь с приемом пищи, частота приема, количество препаратов), нежелательные действия (в том числе легкие, которые, по мнению врача, не требуют отмены препарата) могут спровоцировать больного на прекращение лечения. Как показали результаты фармакоэпидемиологического исследования, примерно 50% взрослых прекращали антибактериальную терапию преждевременно, а более 10% не следовали рекомендуемому режиму дозирования. Среди родителей 18,7% заканчивали антибактериальную терапию у детей преждевременно (не придерживались рекомендуемого врачом курса). Таким образом, результаты проведенного исследования показали, что взрослое население характеризируется неудовлетворительной комплаентностью в отношении рекомендуемой длительности курса антибактериальной терапии [10]. При проведении исследования по оценке сравнительной эффективности коротких (5-дневных) курсов левофлоксацина и 7-дневных было показано, что эффективность первых курсов не отличается от последних: при обоих режимах лечения отмечалась равная клиническая и микробиологическая эффективность [11]. С этих позиций респираторные фторхинолоны, которые можно принимать однократно в сутки, независимо от приема пищи и короткими курсами, имеют преимущества перед многими другими антибактериальными препаратами и их назначение повышает комплаентность пациентов.
Наличие форм для парентерального и перорального введения повышают удобство использования препаратов и делают возможным их использование в режиме ступенчатой терапии.
Клиническая, бактериологическая эффективность и безопасность респираторных фторхинолонов была оценена во многих многоцентровых клинических исследованиях. Так, по данным метаанализа пяти клинических исследований, прием моксифлоксацина в дозе 400 мг 1 раз в сутки при респираторных инфекциях по клинической эффективности не отличался от амоксициллина в дозе 1000 мг 3 раза в сутки и кларитромицина в дозе 500 мг 2 раза в сутки. Бактериологическая эффективность моксифлоксацина была выше и составила 94%. При использовании левофлоксацина при лечении пациентов с пневмонией препарат применяли в суточной дозе 500 мг. В исследование включили 68 больных; у 26 была пневмония тяжелого течения — у них левофлоксацин применяли в режиме ступенчатой терапии. Клиническая и бактериологическая эффективность препарата составила 100%. Только в одном случае (1,4%) потребовалась его отмена из-за преходящих нарушений психики [12]. В исследовании C. Fogarty et al. (1999) эффективность и безопасность терапии моксифлоксацином в дозе 400 мг в сутки в течение 10 дней сравнивали с эффективностью и безопасностью кларитромицина в дозе 500 мг в сутки в течение 10 дней. В исследование были включены 382 пациента с внебольничной пневмонией. Оба препарата оказались сопоставимы как по эффективности, так и по частоте развития нежелательных действий. Эффективность лечения составила 95%. В исследование по сравнению эффективности моксифлоксацина и кларитромицина у больных ХОБЛ были включены 750 пациентов (R. Wilson et al., 1999). Пациенты получали моксифлоксацин в дозе 400 мг/сут в течение 5 дней или кларитромицин в дозе 500 мг 2 раза в сутки в течение 7 дней. Клиническое выздоровление отмечалось у 89% пациентов, получавших моксифлоксацин, и у 88% пациентов, принимавших кларитромицин. Через месяц после окончания курса терапии клиническая эффективность подтверждена у 89% пациентов обеих групп. При этом бактериологическая эффективность моксифлоксацина была достоверно выше: 77,4 и 62,3% соответственно. Российские авторы сравнивали эффективность лечения обострения хронического бронхита левофлоксацином в дозе 500 мг/сут в течение 7 дней и цефуроксим аксетилом в дозе 250 мг 2 раза в сутки в течение 10 дней. Клиническая эффективность препаратов не отличалась и составила 92% в обеих группах, тогда как бактериологическая эффективность была выше в группе принимавших левофлоксацин и составила 94% против 87% в группе лечения цефуроксим аксетилом [14].
В заключение следует отметить, что респираторные фторхинолоны высокоактивны в отношении наиболее распространенных возбудителей пневмонии и обострения хронического бронхита, в том числе штаммов, устойчивых к β-лактамам, макролидам. Препараты обладают высокой биодоступностью при приеме внутрь, быстро всасываются, создают высокие концентрации в легочной ткани, бронхолегочном секрете, в клетках организма человека. Они обладают длительным периодом полувыведения, что позволяет принимать их 1-2 раза в сутки, выпускаются в виде форм для парентерального и перорального приема, что дает возможность использовать их в режиме ступенчатой терапии. Эффективность коротких 5-дневных курсов сопоставима с эффективностью более длительных курсов антибактериальной терапии. Препараты хорошо переносятся, обладают минимальным количеством нежелательных лекарственных и диетических взаимодействий.
По вопросам литературы обращайтесь в редакцию.
Е. А. Прохорович, доктор медицинских наук, профессор
МГМСУ, Москва
- Baas, «Geschichte d. Medicin».
- Bangun H., Aulia F., Arianto A., Nainggolan M. Preparation of mucoadhesive gastroretentive drug delivery system of alginate beads containing turmeric extract and anti-gastric ulcer activity. Asian Journal of Pharmaceutical and Clinical Research. 2019; 12(1):316–320. DOI: 10.22159/ajpcr.2019.v12i1.29715.
- Wunderlich, «Geschichte der Medicin» (Штуттгардт, 1958).
- https://www.rmj.ru/articles/bolezni_dykhatelnykh_putey/Respiratornye_ftorhinolony_pri_lechenii_bronholegochnyh_infekciy/.
- https://www.lvrach.ru/2007/08/4716410.
- Wise, «Review of the History of Medicine» (Л., 1967).
- Moustafine R. I., Bobyleva V. L., Bukhovets A. V., Garipova V. R.,Kabanova T. V., Kemenova V. A., Van den Mooter G. Structural transformations during swelling of polycomplex matrices based on countercharged (meth)acrylate copolymers (Eudragit® EPO/Eudragit® L 100-55). Journal of Pharmaceutical Sciences. 2011; 100:874–885. DOI:10.1002/jps.22320.
- Debjit B., Rishab B., Darsh G., Parshuram R., Sampath K. P. K. Gastroretentive drug delivery systems- a novel approaches of control drug delivery systems. Research Journal of Science and Technology;10(2): 145–156. DOI: 10.5958/2349-2988.2018.00022.0.