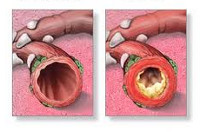
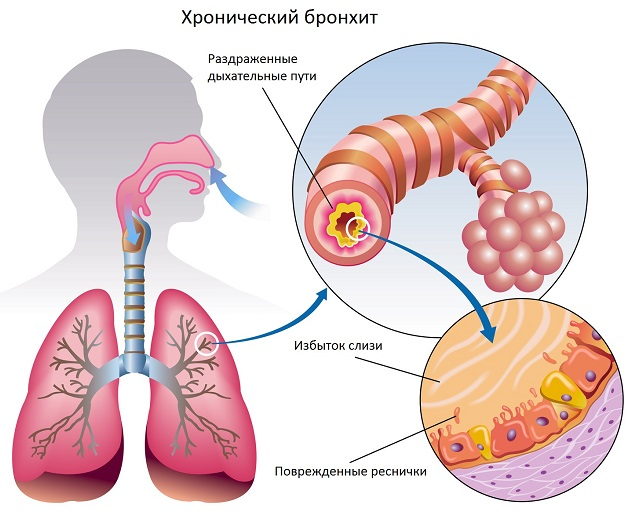
По определению ВОЗ, «Обструкция дыхательных путей — сужение или окклюзия дыхательных путей, которая может быть результатом скопления материала в просвете, утолщения стенки, сокращения бронхиальных мышц, уменьшения сил ретракции легкого, разрушения дыхательных путей без соответствующей потери альвеолярной ткани и/или компрессии дыхательных путей». Клинически нарушения бронхиальной обструкции нижних дыхательных путей у детей раннего возраста, независимо от вызвавшей их причины, проявляются однотипно — остро возникшей экспираторной одышкой в виде шумного дыхания с форсированным удлиненным выдохом, вздутием грудной клетки и втяжением ее уступчивых мест, навязчивым кашлем, вариабельными диффузными сухими и разного калибра влажными хрипами в легких. Рентгенологически определяются признаки вздутия легочной ткани. Функциональными методами выявляется повышенное бронхиальное сопротивление воздушному потоку вследствие диффузного нарушения проходимости мелких бронхов и бронхиол.
Для клинического определения бронхообструктивных нарушений на практике можно встретить самые разнообразные термины: астматический, обструктивный, брохоспастический, астмоидный, бронхообструктивный синдром, астматический компонент, предастма, обструкция дыхательных путей, синдром бронхиальной обструкции и т.д.
Однако наиболее универсальным и предпочтительным является термин «Бронхообструктивный синдром» (БОС).
Термин «Бронхообструктивный синдром» — собирательный и не может служить самостоятельным нозологическим диагнозом.
В каждом конкретном случае должен быть расшифрован ведущий механизм обструкции и решен вопрос об основном заболевании, осложнением или главным клиническим проявлением которого бронхообструктивный синдром является. У детей раннего возраста в силу характерных для них морфо-функциональных особенностей весьма часты явления бронхиальной обструкции инфекционно-воспалительного генеза, возникающие остро на фоне ОРВИ, клинически сходные с проявлениями бронхиальной астмы (БА), но не имеющие прямого отношения к этому диагнозу и являющиеся проявлением обструктивного бронхита. Одновременно различные респираторные вирусы являются важнейшими триггерами БА, особенно,в первые годы жизни.
Бронхиальная астма в этом возрасте клинически часто протекает по типу астматического бронхита, так называемой «влажной астмы» (С.Г.Звягинцева, 1958). Общепризнано нецелесообразным сегодня выделение астматического бронхита в самостоятельную нозологическую форму, т.к. он является клиническим эквивалентом бронхиальной астмы, характерным для детей раннего возраста и соответствующим интермитирующей или персистирующей формам ее, согласно 2 версии (2006г.) Национальной Программы по бронхиальной астме у детей
Среди этиологических факторов ОРВИ, сопровождающихся бронхообструктивным синдромом, отмечаются самые разные инфекционные агенты и их ассоциации: грипп, парагрипп, риновирусы, аденовирусы, респираторно-синцитиальный вирус, цитомегаловирусы, вирус кори, микоплазмы, хламидии, Echo- и Коксаки вирусы, легионеллы, пневмоцисты.
Патофизиологические механизмы БОС при ОРВИ
- Отек и инфильтрация бронхиальной стенки (вследствие вирусного воспаления)
- Гиперсекреция слизи и десквамация реснитчатого эпителия, ведущие к нарушению мукоцилиарного клиренса
- Бронхоспазм, развивающийся как под действием биологически активных веществ, выделяемых в ходе воспалительной реакции, так и нервно-рефлекторно при непосредственном воздействии вирусов на нервные окончания, бета-2-адренорецепторы.
Морфо-функциональные особенности детей раннего возраста, способствующие развитию БОС:
- узость дыхательных путей
- податливость хрящей и ригидность грудной клетки
- меньшая эластичность легочной ткани
- обильная васкуляризация
- склонность к отеку и экссудации
У ребенка старше 4-5 лет инфекционный генез повторных бронхообструктивных эпизодов возможен только как казуистика. Совершенно очевидно, что вероятность чисто инфекционного генеза обструкции уменьшается с возрастом ребенка, а вероятность аллергического заболевания (бронхиальной астмы) возрастает.
У большинства ( 80 %) больных бронхиальной астмой, ее дебют относится к раннему возрасту, т.е. первым трем годам жизни. Однако диагностика болезни в этом периоде в силу ряда объективных причин трудна. Длительное время скрываясь под маской «острой респираторной инфекции с обструктивным синдромом» или «обструктивного бронхита», бронхиальная астма своевременно не распознается и больные, соответственно, не лечатся. Лишь спустя годы у части детей обнаруживается переход так называемого рецидивирующего обструктивного бронхита в типичную бронхиальную астму.
Принципиально важными условиями развития БА являются: наследственная предрасположенность, атопия и гиперреактивность бронхов.
Потенциальными критериями диагностики бронхиальной астмы в раннем детском возрасте являются:
1. Повторные эпизоды бронхиальной обструкции как на фоне ОРВИ, так и вне их
2. Отчетливый положительный эффект бронхолитической терапии
3. Наследственная отягощенность аллергическими заболеваниями
4. Наличие сопутствующих аллергических заболеваний (атопический дерматит, аллергический ринит, проявления пищевой и лекарственной аллергии)
5. Эозинофилия в крови
6. Высокий уровень IgE в крови
7. Наличие в крови специфических IgE к различным аллергенам
Безусловно, не существует каких-либо патогномоничных симптомов, позволяющих диагностировать бронхиальную астму в раннем возрасте. Однако, совокупная оценка характерных признаков с высокой долей вероятности позволяет устанавливать этот диагноз уже на ранних этапах заболевания.
Дифференциальный диагноз бронхиальной астмы у детей раннего возраста следует проводить со следующими заболеваниями:
- Обструктивный бронхит при острой респираторной инфекции
- Муковисцидоз
- Гастроэзофагеальная рефлюксная болезнь
- Первичная цилиарная дискинезия
- Пороки развития легких, трахеобронхомегалия, Синдром Вильямса-Кэмпбелла, сдавление аномальными крупными сосудами, бронхами , бронхогенные кисты
- Врожденные пороки сердца, приводящие к синдрому сдавления
- Новообразования средостения
- Инородное тело трахеи и бронхов
- Облитерирующий бронхиолит
- Папиллома подсвязочного пространства гортани
- Карциноид трахеи
- Новообразования средостения
- Сдавление увеличенным тимусом
- Короткий пищевод
- Диафрагмальная грыжа
- Дыхательный невроз
- Аллергический бронхолегочный аспергиллез, аллергический бронхит, экзогенный аллергический альвеолит.
Научно-практическими наблюдениями последних лет установлено, что бронхо-легочная дисплазия (БЛД) в хронической стадии заболевания должна быть включена в дифференциально-диагностический поиск при обструктивных заболеваниях легких ( Д.Ю. Овсянников и соавт., 2006 г.). Наши данные (А.В.Кузнецова), касающиеся катамнестического наблюдения 27 недоношенных детей с периода новорожденности до 1 года и имевших клинические проявления БЛД с 3 — 4 недель жизни подтверждают это: БОС в дебюте БЛД констатирован у 13 (48,1%) на фоне текущей и повторной пневмонии, стенозирующего ларингита и трахеобронхита, клиника хронической дыхательной недостаточности на фоне рецидивирующего обструктивного бронхита (и его наиболее тяжелого варианта — бронхиолита) после снятия с ИВЛ в связи с тяжелой формой респираторного дистресс-синдрома у 14 (51,85%)пациентов, у 3 из них наблюдалась типичная клинико-лабораторная панорама БА.
Принципы терапии острой бронхиальной обструкции у детей:
1. При любой обструкции дыхательных путей важно как можно более раннее начало лечения.
2. Адекватная регидратация и (при необходимости) кислородная поддержка
3. Бронхолитическая терапия наиболее оптимальна в ингаляциях через небулайзер (в качестве препарата первого выбора — беродуал, представляющий собой комбинацию бета2-агониста (Фенотерола гидробромида) и холиноблокатора (Ипратропия бромида). 1 мл раствора для ингаляций содержит 20 капель беродуала; в 1 капле 25 мкг фенотерола и 12,5 мкг ипратропия бромида. Необходимую дозу разводят в 2-4 мл физиологического раствора и ингалируют через небулайзер с неплотной маской. Разводить дистиллированной водой нельзя!
Дозы беродуала: Детям до 6 лет назначают на 1 ингаляцию: 0,5 мл (10 кап)
или 2 кап/кг массы, но не более 10 кап. Детям 6-14 лет назначают на 1 ингаляцию 0,5-1,0 мл (10-20 кап). Интервал между ингаляциями 4-6 час
При отсутствии небулайзера возможно ингалировать беродуал через спейсер.
Преимуществами новой бесфреоновой формы дозированного аэрозоля Беродуал® Н являются:
— улучшенная воспроизводимость дозы;
— проще техника ингаляции;
— нет охлаждающего действия фреона;
— более мелкий размер частиц.
Безусловно, в качестве бронхолитика могут быть использованы и другие симпатомиметики (сальбутамол и др.), как через небулайзер, так и в инъекциях (п/к, в/м) или внутрь.
Приводим собственные данные сравнительного клинического использования сальбутамола и беродуала в небулайзерной терапии БОС у детей с БЛД на первом году жизни (А.В.Кузнецова):
— на фоне применения сальбутамола у 13 больных детей длительность БОС составила 4,56+0,41 дня,
— применение беродуала у 14 детей, причем у 6 из них ранее был использован сальбутамол, способствовало сокращению длительности БОС до 3,14+0,35дней (р<0,05). В крайнем случае может быть использован и метилксантиновый препарат — эуфиллин (с известными предосторожностями).
У детей, особенно раннего возраста, беродуал всё же предпочтительнее других симпатомиметиков, поскольку он содержит комбинацию бета2-агониста (Фенотерола гидробромида) и холиноблокатора (Ипратропия бромида), влияющих на различные механизмы бронхоконстрикции.
Беродуал оптимален для борьбы с обструкцией любой этиологии, высоко эффективен, риск развития осложнений/побочных эффектов терапии максимально низок.
В соответствии с тяжестью состояния — кортикостероидная терапия: желательно ингаляционная — суспензия будесонида (пульмикорт) через небулайзер. Рекомендуемые дозы будесонида суспензии (пульмикорта) в ингаляциях: Дети 6 месяцев и старше -начальная дозировка 0,25-0,5 мг/сут, дозировка при поддерживающем лечении -0,25-2 мг/сут. Эффективность терапии обострений БА у детей (1,5 — 14 лет) при использовании Пульмикота суспензии достигается в более короткие сроки, чем при назначении системных стероидов (p<0,05). При этом весьма высоко эффективным и оптимальным является сочетание в одной небулайзерной ингаляции беродуала и пульмикорта.
При отсутствии возможности ингалировать кортикостероиды через небулайзер можно использовать ИКС через спейсер, преднизолон (гидрокортизон, дексаметазон) в инъекциях (в/м, в/в) или преднизолон внутрь. Следует воздержаться от применения горчичников и т.п. Всё шире в последнее время в качестве противовоспалительного средства при ОРВИ, в т.ч. с бронхообструктивным синдромом, в педиатрии используется фенспирид (эреспал).
Муколитическая терапия при обструкции у детей раннего и дошкольного возраста совершенно необходима, но имеет свои нюансы.
Наличие бронхиальной обструкции всегда ухудшает эвакуацию мокроты и требует сочетанного с бронхолитиками назначения отхаркивающих средств и обязательного увлажнения дыхательных путей. При этом использование антигистаминных (I поколения) и атропиноподобных средств у детей нецелесообразно, так как обладает «подсушивающим» слизистую оболочку эффектом, сгущает мокроту и затрудняет ее эвакуацию. Наиболее современ- ными и эффективными муколитиками являются препараты на основе амброксола, в частности лазолван и амбробене.
Лазолван нашел особенную терапевтическую нишу применения у новорожденных и, в частности, у недоношенных детей с респираторным дистресс-синдромом (РДС) в тех случаях, когда нет реальной возможности введения сурфактанта в первые часы жизни, а также при БОС у новорожденных с риском БЛД. Так, средняя длительность пребывания новорожденных пациентов с РДС на ИВЛ, в комплексной терапии которых использован лазолван в форме ингаляций, была лишь на 2,82+0,91 дня больше, чем при использовании сурфактанта. (А.В.Кузнецова и соавт.,).
В последнее время довольно популярны комбинированные препараты, которые могут включать различные отхаркивающие, противокашлевые, спазмолитические и другие средства. Однако, следует иметь ввиду, что их назначение требует индивидуального подхода, а сочетания препаратов в них не всегда рациональны.
Для эффективной эвакуации мокроты в комплексе лечения детей с бронхолегочной патологией целесообразно также использовать ингаляции, постуральный и вибрационный массаж. Применение отхаркивающих средств должно сочетаться с назначением обильного питья (минеральная вода, чай, компот, морс, отвар сухофруктов и т.д.). Иногда при назначении отхаркивающих препаратов происходит непредсказуемо резкое снижение вязкости и значительное увеличение количества отделяемой мокроты, что приводит к ухудшению бронхиальной проходимости. Клинически это проявляется усилением кашля, одышки, ухудшением общего состояния ребенка. В этих случаях необходима отмена или снижение дозы отхаркивающих средств. У детей раннего возраста, а также при выраженном рвотном рефлексе и высоком риске аспирации, противопоказаны отхаркивающие препараты, увеличивающие объем секрета, усиливающие рвотный и кашлевой рефлексы.
Антибиотикотерапия применяется по строгим показаниям (лихорадка выше 38 град. более 2-3-х дней, выраженная интоксикация, невозможность исключить бактериальные осложнения, прежде всего пневмонию, бронхит).
С профилактической целью у детей старше 2,5 лет возможно применение (по показаниям) только местных антибактериальных средств — ингаляционно фузафунжин . В реанимационных случаях необходима поддержка сердечной деятельности, коррекция электролитов, антикоагулянты (под контролем коагулограммы, ТЭГ). В раннем возрасте, как ни в каком другом, необходим учет и коррекция фоновых патологических состояний.
Если причиной обструкции явилась бронхиальная астма ребенок нуждается в профилактической (базисной) терапии, что решается специалистом в соответствии с характером и тяжестью течения болезни. В раннем возрасте с этой целью достаточно эффективны кетотифен, задитен, кромоны. При необходимости могут назначаться ИКС (флютиказон с 1 года, пульмикорт с 6 мес).
Безусловно, необходимо оздоровление домашней среды, исключение пассивного курения, контактов с причинно значимыми аллергенами, гипоаллергенная диета, индивидуальный график прививок, санация носоглотки, лечение сопутствующей аллергической (алл.ринит, атоп. дерматит) и иной патологии, всемерная профилактика ОРЗ (закаливание, адаптогены, иммунокорректоры), общеоздоровительные мероприятия (ЛФК, массаж и т.д.)
Ю.Л. Мизерницкий, А.В.Кузнецова
Московский НИИ педиатрии и детской хирургии Росздрава,
Казанская государственная медицинская академия
Мизерницкий Юрий Леонидович — профессор,. Руководитель отделения пульмонологии Московского НИИ педиатрии и детской хирургии Росздрава, главный детский пульмонолог Минздрава РФ.
Литература:
1. Звягинцева С.Г.Бронхиальная астма у детей.М.: Медгиз,1958.
2.Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». Москва, 2006.
3.Овсянников Д.Ю.,Кузьменко Л.Г.,Зайцева Э.Г. Бронхолегочная дисплазия в хронической стадии у детей грудного и раннего возраста. Пульмонология детского возраста: проблемы и решения, в.6, Москва, 2006, с.8 — 15.
Обструктивный бронхит у детей
Обструктивный бронхит у детей — воспалительное поражение бронхиального дерева, протекающее с явлением обструкции, т. е. нарушением проходимости бронхов. Течение обструктивного бронхита у детей сопровождается малопродуктивным кашлем, шумным свистящим дыханием с форсированным выдохом, тахипноэ, дистанционными хрипами. При диагностике обструктивного бронхита у детей учитываются данные аускультации, рентгенографии грудной клетки, спирометрии, бронхоскопии, исследования крови (общего анализа, газов крови). Лечение обструктивного бронхита у детей проводится с помощью ингаляционных бронхолитиков, небулайзерной терапии, муколитиков, массажа, дыхательной гимнастики.
Общие сведения
Бронхиты у детей являются самими распространенными заболеваниями респираторного тракта. У детей раннего возраста воспаление бронхов нередко протекает с бронхообструктивным синдромом, обусловленным отеком слизистой, повышенной бронхиальной секрецией и бронхоспазмом. В первые три года жизни обструктивный бронхит переносят около 20% детей; у половины из них в дальнейшем эпизоды бронхообструкции повторяются, как минимум 2-3 раза.
Дети, неоднократно болеющие острыми и обструктивными бронхитами, составляют группу риска по развитию хронической бронхолегочной патологии (хронического бронхита, облитерирующего бронхиолита, бронхиальной астмы, бронхоэктатической болезни, эмфиземы легких). В связи с этим вопросы трактовки этиологии и патогенеза, клинического течения, дифференциальной диагностики и современного терапевтического лечения являются приоритетными для педиатрии и детской пульмонологии.
Обструктивный бронхит у детей
Причины
В этиологии обструктивного бронхита у детей первостепенную роль играют респираторно-синцитиальный вирус, вирус парагриппа 3 типа, энтеровирусы, вирусы гриппа, адено- и риновирусы. Подтверждением ведущего значения вирусных возбудителей служит тот факт, что в большинстве наблюдений манифестации обструктивного бронхита у ребенка предшествует ОРВИ.
При повторных эпизодах обструктивного бронхита у детей в смыве с бронхов часто выявляется ДНК персистирующих инфекций — хламидий, микоплазм, герпесвирусов, цитомегаловируса. Часто бронхит с обструктивным синдромом у детей провоцируется плесневым грибком, который интенсивно размножается на стенах помещений с повышенной влажностью. Оценить этиологическое значение бактериальной флоры довольно затруднительно, поскольку многие ее представители выступают условно-патогенными компонентами нормальной микрофлоры дыхательных путей.
Немаловажную роль в развитии обструктивного бронхита у детей играет аллергический фактор — повышенная индивидуальная чувствительность к пищевым продуктам, лекарственным препаратам, домашней пыли, шерсти животных, пыльце растений. Именно поэтому обструктивному бронхиту у детей часто сопутствуют аллергический конъюнктивит, аллергический ринит, атопический дерматит.
Рецидивам эпизодов обструктивного бронхита у детей способствует глистная инвазия, наличие очагов хронической инфекции (синуситов, тонзиллита, кариеса и др.), активное или пассивное курение, вдыхание дыма, проживание в экологически неблагоприятных регионах и т. д.
Патогенез
Патогенез обструктивного бронхита у детей сложен. Вторжение вирусного агента сопровождается воспалительной инфильтрацией слизистой бронхов плазматическими клетками, моноцитами, нейтрофилами и макрофагами, эозинофилами. Выделение медиаторов воспаления (гистамина, простагландинов и др.) и цитокинов приводит к отеку бронхиальной стенки, сокращению гладкой мускулатуры бронхов и развитию бронхоспазма.
Вследствие отека и воспаления увеличивается количество бокаловидных клеток, активно вырабатывающих бронхиальный секрет (гиперкриния). Гиперпродукция и повышенная вязкость слизи (дискриния) вызывают нарушение функции реснитчатого эпителия и возникновение мукоцилиарной недостаточности (мукостаза). Вследствие нарушения откашливания, развивается обтурация дыхательных путей бронхиальным секретом. На этом фоне создаются условия для дальнейшего размножения возбудителей, поддерживающих патогенетические механизмы обструктивного бронхита у детей.
Некоторые исследователи в бронхообструкции видят не только нарушение процесса внешнего дыхания, но и своего рода приспособительные реакции, которые в условиях поражения реснитчатого эпителия защищают легочную паренхиму от проникновения в нее патогенов из верхних дыхательных путей. Действительно, в отличие от простого бронхита, воспаление с обструктивным компонентом значительно реже осложняется пневмонией у детей.
Для обозначения обструктивного бронхита у детей иногда используются термины «астматический бронхит» и «спастический бронхит», однако они являются более узкими и не отражают всей полноты патогенетических механизмов заболевания.
По течению обструктивный бронхит у детей может быть острым, рецидивирующим и хроническим или непрерывно-рецидивирующим (при бронхолегочной дисплазии, облетирующем бронхиолите и др.). По степени выраженности бронхиальной обструкции выделяют: легкую (I), среднетяжелую (II), тяжелую (III) степень обструктивного бронхита у детей.
Симптомы обструктивного бронхита у детей
Чаще всего первый эпизод обструктивного бронхита развивается у ребенка на 2-3-м году жизни. В начальном периоде клиническая картина определяется симптомами ОРВИ — повышенной температурой тела, першением в горле, насморком, общим недомоганием. У детей раннего возраста нередко развиваются диспептические симптомы.
Бронхиальная обструкция может присоединяться уже в первые сутки заболевания или через 2-3 дня. При этом отмечается увеличение частоты дыхания (до 50-60 в мин.) и продолжительности выдоха, который становится шумным, свистящим, слышимым на расстоянии. Кроме тахипноэ, экспираторной или смешанной одышки у детей с обструктивным бронхитом отмечается задействованность в акте дыхания вспомогательной мускулатуры, увеличение переднезаднего размера грудной клетки, втяжение ее уступчивые мест при дыхании, раздувание крыльев носа. Кашель у детей с обструктивным бронхитом малопродуктивный, со скудной мокротой, иногда мучительный, приступообразный, не приносящий облегчения. Даже при влажном кашле мокрота отходит с трудом. Отмечается бледность кожных покровов или периоральный цианоз. Проявления обструктивного бронхита у детей могут сопровождаться шейным лимфаденитом. Бронхообструкция держится 3-7 дней, исчезает постепенно по мере стихания воспалительных изменений в бронхах.
У детей первого полугодия, особенно соматически ослабленных и недоношенных, может развиваться наиболее тяжелая форма обструктивного синдрома — острый бронхиолит, в клинике которого преобладают признаки тяжелой дыхательной недостаточности. Острый обструктивный бронхит и бронхиолит нередко требуют госпитализации детей, поскольку данные заболевания приблизительно в 1% случаев заканчиваются летальным исходом. Затяжное течение обструктивного бронхита наблюдается у детей с отягощенным преморбидным фоном: рахитом, хронической ЛОР-патологией, астенизацией, анемией.
Диагностика
Клинико-лабораторное и инструментальное обследование детей с обструктивным бронхитом проводится педиатром и детским пульмонологом; по показаниям ребенку назначаются консультации детского аллерголога-иммунолога, детского отоларинголога и других специалистов. При аускультации выслушивается удлиненный выдох, разнокалиберные влажные и рассеянные сухие хрипы с двух сторон; при перкуссии над легкими определяется коробочный оттенок.
На рентгенограммах органов грудной клетки выражены признаки гипервентиляции: повышение прозрачности легочной ткани, горизонтальное расположение ребер, низкое стояние купола диафрагмы. В общем анализе крови может выявляться лейкопения, лимфоцитоз, небольшое увеличение СОЭ, эозинофилия. При исследовании газового состава крови обнаруживается умеренная гипоксемия. В случае необходимости дополнительно проводится иммунологическое, серологическое, биохимическое исследование крови; определение ДНК основных респираторных патогенов в крови методом ПЦР, постановка аллергологических проб. Выявлению возбудителей могут способствовать микроскопическое исследование мокроты, бакпосев мокроты на микрофлору, исследование смывов из носоглотки.
При обструктивном бронхите у детей необходимо исследование дыхательных объемов (ФВД), в том числе с лекарственными пробами. С целью визуальной оценки состояния слизистой оболочки бронхов, проведения бронхоальвеолярного лаважа, цитологического и бактериологического исследования промывных вод детям с обструктвиным бронхитом выполняется бронхоскопия.
Повторные эпизоды обструктивного бронхита требуют дифференциальной диагностики с бронхиальной астмой у детей.
Лечение обструктивного бронхита у детей
Терапия обструктивного бронхита у детей раннего возраста проводится в стационаре; более старшие дети подлежат госпитализации при тяжелом течении заболевания. Общие рекомендации включают соблюдение полупостельного режима и гипоаллергенной (преимущественно молочно-растительной) диеты, обильное питье (чаи, отвары, морсы, щелочные минеральные воды). Важными режимными моментами служат увлажнение воздуха, регулярная влажная уборка и проветривание палаты, где лечатся дети с обструктивным бронхитом.
При выраженной бронхообструкции активно применяется кислородотерапия, горячие ножные ванны, баночный массаж, удаление слизи из верхних дыхательных путей электроотсосом. Для снятия обструкции целесообразно использовать ингаляции адреномиметиков (сальбутамола, тербуталина, фенотерола) через небулайзер или спейсер. При неэффективности бронхолитиков лечение обструктивного бронхита у детей дополняется кортикостероидами.
Для разжижения мокроты показано применение препаратов с муколитическим и отхаркивающим эффектами, лекарственных и щелочных ингаляций. При обструктивном бронхите детям назначаются спазмолитические и противоаллергические средства. Антибактериальная терапия проводится только в случае присоединения вторичной инфекции.
С целью обеспечения адекватного дренажа бронхиального дерева детям с обструктивным бронхитом показана дыхательная гимнастика, вибрационный массаж, постуральный дренаж.
Прогноз и профилактика
Около 30-50% детей склонны к повторению обструктивного бронхита в течение одного года. Факторами риска рецидива бронхообструкции служат частые ОРВИ, наличие аллергии и очагов хронической инфекции. У большинства детей эпизоды обструкции прекращаются в дошкольном возрасте. Бронхиальная астма развивается у четверти детей, перенесших рецидивирующий обструктивный бронхит.
К мерам профилактики обструктивного бронхита у детей относится предупреждение вирусных инфекций, в том числе при помощи вакцинации; обеспечение гипоаллергенной среды, закаливание, оздоровление на климатических курортах. После перенесенного обструктивного бронхита дети находятся на диспансерном наблюдении у педиатра, возможно — детского пульмонолога и аллерголога.
- Puccinotti, «Storia della medicina» (Ливорно, 1954—1959).
- Sprengel, «Pragmatische Geschichte der Heilkunde».
- Puccinotti, «Storia della medicina» (Ливорно, 1954—1959).
- https://mfvt.ru/sovremennye-podxody-k-terapii-ostroj-bronxialnoj-obstrukcii-u-detej/.
- https://www.KrasotaiMedicina.ru/diseases/children/obstructive-bronchitis.
- М.П. Киселева, З.С. Шпрах, Л.М. Борисова и др. Доклиническое изучение противоопухолевой активности производного N-гликозида индолокарбазола ЛХС-1208. Сообщение II // Российский биотерапевтический журнал. 2015. № 3. С. 41-47.
- Мустафин Р. И., Протасова А. А., Буховец А. В., Семина И.И. Исследование интерполимерных сочетаний на основе (мет)акрилатов в качестве перспективных носителей в поликомплексных системах для гастроретентивной доставки. Фармация. 2014; 5: 3–5.
- Bangun H., Aulia F., Arianto A., Nainggolan M. Preparation of mucoadhesive gastroretentive drug delivery system of alginate beads containing turmeric extract and anti-gastric ulcer activity. Asian Journal of Pharmaceutical and Clinical Research. 2019; 12(1):316–320. DOI: 10.22159/ajpcr.2019.v12i1.29715.